Белки. Термины | Учеба-Легко.РФ — крупнейший портал по учебе
Белки — это высокомолекулярные вещества органической природы, состоящие из структурных элементов — аминокислот. За счет наличия белков в организме осуществляются построение различных клеточных и внеклеточных структурных элементов, транспорт различных веществ (транспортные белки крови, транспортные белки мембран и т. д.), регуляция различных обменных процессов в организме (гормоны). Белки выполняют защитную функцию, что связано с белковой природой антител, белковой природой противосвертывающей системы крови.
Каталитическая функция белков связана с белковой природой ферментов. Ферменты увеличивают скорость химических реакций.
Сократительная функция белков связана с такими белками, как актин и миозин. Энергетическая функция белков связана с тем, что при полном расщеплении белковой молекулы происходит выделение 17,6 кДж энергии.
Аминокислоты — структурные единицы белковой молекулы, состоящие из карбоксильной группы, обладающей кислотными свойствами, аминогруппы, обладающей основными свойствами, и радикала.
Нейтральные аминокислоты — аминокислоты, в составе которых содержится по одной карбоксильной и аминогруппе.
Кислые аминокислоты — аминокислоты, в составе которых содержится более одной карбоксильной группы.
Основные аминокислоты — аминокислоты, в составе которых содержится более одной аминогруппы.
Заменимые аминокислоты — аминокислоты, которые образуются в организме. Незаменимые аминокислоты не образуются в дан- ном организме, для жизнедеятельности организма необходимо поступление их в достаточном количестве с продуктами питания.
Структура белковой молекулы — сложная пространственная структура, обладающая первичным, вторичным, третичным и четвертичным уровнями организации. Особенности структурной организации белковой молекулы определяются первичным уровнем ее организации.
Первичная структура белковой молекулы — полипептидная цепь с линейной последовательностью аминокислот, связанных между собой за счет пептидной связи. Первичная структура белка наиболее прочная из всех. В отношении всех свойств, которыми будет обладать белковая молекула, эта структура является определяющей. Все остальные структурные уровни организации образуются в соответствии с особенностями строения первичного уровня по принципу самосборки. Внешние факторы не оказывают влияния на этот процесс.
Вторичная структура белковой молекулы — структура белковой молекулы, образующаяся за счет скручивания линейной последовательности аминокислот первичной структуры с образованием спирали, многочисленные витки которой связаны между собой водородными связями.
Третичная структура белковой молекулы — структура белковой молекулы, образующаяся за счет наложения одних частей спирали белковой молекулы на другие, формирования между этими частями различного рода связей: водородных ковалентных ионных, дисульфидных (при наличии аминокислоты цистеин), гидрофобных. Третичная структура имеет вид глобулы.
При третичном уровне организации белковой молекулы возможность принимать участие в химических реакциях, проявлять химическую активность остается только у тех аминокислотных остатков, которые имеют поверхностное расположение.
Четвертичная структура белковой молекулы — структура белковой молекулы, представляющая собой сложную пространственную организацию нескольких полипептидных цепей, связанных между собой за счет различных химических связей. Эти связи аналогичны таковым в третичном уровне организации белковой молекулы. Полипептидные цепи, принимающие участие в образовании четвертичной структуры белковой молекулы, могут быть одинаковыми или иметь различное строение.
Денатурация белков — процесс, при котором происходит нарушение структурной организации белковой молекулы. Денатурация может происходить под влиянием различных факторов.
Денатурация может быть обратимой, когда происходит сохранение первичной структуры белковой молекулы и возможно восстановление полноценной структуры белка. Этот вид денатурации имеет чрезвычайно важное значение в процессе выполнения белками различных функций в организме. Необратимая денатурация характеризуется нарушениями в первичной структуре белка, когда восстановление белковой структуры становится невозможным.
Ренатурация — процесс восстановления структурной организации белковой молекулы. Ренатурация возможна только при обратимой денатурации.
Ферменты — вещества белковой природы, за счет наличия которых обеспечивается ускорение реакций, протекающих в организме. Скорость этих реакций при отсутствии ферментов была бы чрезвычайно мала.
Для ускорения реакции необходимо очень небольшое количество фермента. Ферменты обладают рядом свойств: ферменты являются глобулярными белками, обеспечивают ускорение скорости реакций, протекающих в организме, количество ферментов до и после реакции не изменяется, определенный фермент катализирует определенную реакцию или определенную группу реакций, т. е. обладает специфичностью. Активность ферментов может быть различна. Влияние на активность ферментов могут оказывать различные факторы среды, в которой протекает реакция: кислотность среды, температура, давление. Большое значение также имеет количество субстрата реакции и самого фермента.
Энергия активации — то количество энергии, которое необходимо, чтобы реакция началась. Ферменты обеспечивают снижение энергии активации.
Фермент-субстратный комплекс — соединение, образующееся при взаимодействии субстрата и фермента, что необходимо для обеспечения катализируемой реакции. за счет наличия активного центра фермента, который и взаимодействует с субстратом.
Специфичность ферментов обеспечивается определенной структурой его активного центра, который должен соответство- вать структуре молекулы субстрата по принципу «ключ-замок».
Кофакторы — вещества небелковой природы, которые необходимы некоторым ферментам для обеспечения их активной работы. Выделяют три группы кофакторов — неорганические ионы, протетические группы и коферменты.
Голофермент — комплекс, образующийся при взаимодействии фермента с кофактором.
Апофермент — часть голофермента без кофактора.
Ингибиторы — вещества, которые препятствуют протеканию ферментативных реакций. Ингибирование может быть обратимым и необратимым. При обратимом ингибировании ингибитор не вступает в реакцию с субстратом, но препятствует осуществлению ферментативной реакции за счет взаимодействия с активным центром фермента.
Необратимое ингибирование — ингибирование ферментативной реакции, когда ингибитор соединяется с неактивной частью фермента, изменяя таким образом его структурную организацию, и создает невозможные условия для осуществления реакции.
uclg.ru
Состав и строение белков
В основе жизнедеятельности клетки лежат биохимические процессы, протекающие на молекулярном уровне и служащие предметом изучения биохимии. Соответственно и явления наследственности и изменчивости тоже связаны с молекулами органических веществ, и в первую очередь с нуклеиновыми кислотами и белками.
Состав белков
Белки представляют собой большие молекулы, состоящие из сотен и тысяч элементарных звеньев — аминокислот. Такие вещества, состоящие из повторяющихся элементарных звеньев — мономеров, называются полимерами. Соответственно белки можно назвать полимерами, мономерами которых служат аминокислоты.
Всего в живой клетке известно 20 видов аминокислот. Название аминокислоты получили из-за содержания в своем составе аминной группы NHy, обладающей основными свойствами, и карбоксильной группы СООН, имеющей кислотные свойства. Все аминокислоты имеют одинаковую группу Nh3—СН—СООН и отличаются друг от друга химической группой, называемой радикалом — R. Соединение аминокислот в полимерную цепь происходит благодаря образованию пептидной связи (СО — NH) между карбоксильной группой одной аминокислоты и аминогруппой другой аминокислоты. При этом выделяется молекула воды. Если образовавшаяся полимерная цепь короткая, она называется олигопептидной, если длинная — полипептидной.
Строение белков
При рассмотрении строения белков выделяют первичную, вторичную, третичную структуры.
Первичная структура определяется порядком чередования аминокислот в цепи. Изменение в расположении даже одной аминокислоты ведет к образованию совершенно новой молекулы белка. Число белковых молекул, которое образуется при сочетании 20 разных аминокислот, достигает астрономической цифры.
Если бы большие молекулы (макромолекулы) белка располагались в клетке в вытянутом состоянии, они занимали бы в ней слишком много места, что затруднило бы жизнедеятельность клетки. В связи с этим молекулы белка скручиваются, изгибаются, свертываются в самые различные конфигурации. Так на основе первичной структуры возникает
Спираль вторичной структуры укладывается в клубок, образуя третичную структуру. Форма клубка у каждого вида белков строго специфична и полностью зависит от первичной структуры, т. е. от порядка расположения аминокислот в цепи. Третичная структура удерживается благодаря множеству слабых электростатических связей: положительно и отрицательно заряженные группы аминокислот притягиваются и сближают даже далеко отстоящие друг от друга участки белковой цепи. Сближаются и иные участки белковой молекулы, несущие, например, гидрофобные (водоотталкивающие) группы.
Некоторые белки, например гемоглобин, состоят из нескольких цепей, различающихся по первичной структуре. Объединяясь вместе, они создают сложный белок, обладающий не только третичной, но и четвертичной структурой (рис. 2).
В структурах белковых молекул наблюдается следующая закономерность: чем выше структурный уровень, тем слабее поддерживающие их химические связи. Связи, образующие четвертичную, третичную, вторичную структуру, крайне чувствительны к физико-химическим условиям среды, температуре, радиации и т. д. Под их воздействием структуры молекул белков разрушаются до первичной — исходной структуры. Такое нарушение природной структуры белковых молекул называется денатурацией. При удалении денатурирующего агента многие белки способны самопроизвольно восстанавливать исходную структуру. Если же природный белок подвергается действию вьюокой температуры или интенсивному действию других факторов, то он необратимо денатурируется. Именно фактом наличия необратимой денатурации белков клеток объясняется невозможность жизни в условиях очень высокой температуры.
Первичная структура белков.
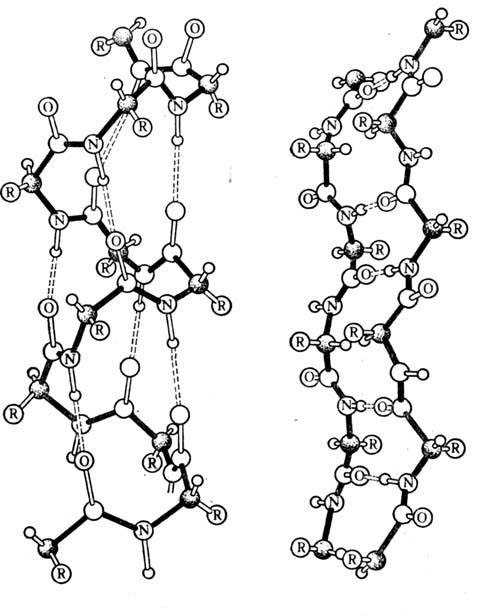
Вторичная структура белков.

Третичная структура белков.
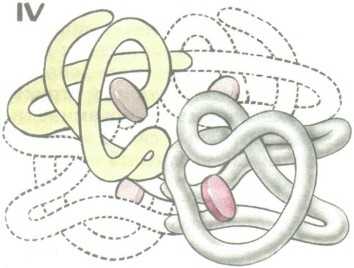
Четвертичная структура белков.
Биологическая роль белков в клетке
Белки, называемые также протеинами (греч. протос — первый}, в клетках животных и растений выполняют многообразные и очень важные функции, к которым можно отнести следующие.
Каталитическая. Природные катализаторы — ферменты представляют собой полностью или почти полностью белки. Благодаря ферментам химические процессы в живых тканях ускоряются в сотни тысяч или в миллионы раз. Под их действием все процессы идут мгновенно в «мягких» условиях: при нормальной температуре тела, в нейтральной для живой ткани среде. Быстродействие, точность и избирательность ферментов несопоставимы ни с одним из искусственных катализаторов. Например, одна молекула фермента за одну минуту осуществляет реакцию распада 5 млн. молекул пероксида водорода (Н202). Ферментам характерна избирательность. Так, жиры расщепляются специальным ферментом, который не действует на белки и полисахариды (крахмал, гликоген). В свою очередь, фермент, расщепляющий только крахмал или гликоген, не действует на жиры.
Процесс расщепления или синтеза любого вещества в клетке, как правило, разделен на ряд химических операций. Каждую операцию выполняет отдельный фермент. Группа таких ферментов составляет биохимический конвейер.
Считают, что каталитическая функция белков зависит от их третичной структуры, при ее разрушении каталитическая активность фермента исчезает.
Защитная. Некоторые виды белков защищают клетку и в целом организм от попадания в них болезнетворных микроорганизмов и чужеродных тел. Такие белки носят название антител. Антитела связываются с чужеродными для организма белками бактерий и вирусов, что подавляет их размножение. На каждый чужеродный белок организм вырабатывает специальные «антибелки» — антитела. Такой механизм сопротивления возбудителям заболеваний называется иммунитетом.
Чтобы предупредить заболевание, людям и животным вводят ослабленные или убитые возбудители (вакцины), которые не вызывают болезнь, но заставляют специальные клетки организма производить антитела против этих возбудителей. Если через некоторое время болезнетворные вирусы и бактерии попадают в такой организм, они встречают прочный защитный барьер из антител.
Гормональная. Многие гормоны также представляют собой белки. Наряду с нервной системой гормоны управляют работой разных органов (и всего организма) через систему химических реакций.
Отражательная. Белки клетки осуществляют прием сигналов, идущих извне. При этом различные факторы среды (температурный, химический, механический и др.) вызывают изменения в структуре белков — обратимую денатурацию, которая, в свою очередь, способствует возникновению химических реакций, обеспечивающих ответ клетки на внешнее раздражение. Эта способность белков лежит в основе работы нервной системы, мозга.
Двигательная. Все виды движений клетки и организма: мерцание ресничек у простейших, сокращение мышц у высших животных и другие двигательные процессы — производятся особым видом белков.
Энергетическая. Белки могут служить источником энергии для клетки. При недостатке углеводов или жиров окисляются молекулы аминокислот. Освободившаяся при этом энергия используется на поддержание процессов жизнедеятельности организма.
Транспортная. Белок гемоглобин крови способен связывать кислород воздуха и транспортировать его по всему телу. Эта важнейшая функция свойственна и некоторым другим белкам.
Пластическая. Белки — основной строительный материал клеток (их мембран) и организмов (их кровеносных сосудов, нервов, пищеварительного тракта и др.). При этом белки обладают индивидуальной специфичностью, т. е. в организмах отдельных людей содержатся некоторые, характерные лишь для него, белки-
Таким образом, белки — эти важнейший компонент клетки, без которого невозможно проявление свойств жизни. Однако воспроизведение живого, явление наследственности, как мы увидим позже, связано с молекулярными структурами нуклеиновых кислот. Это открытие — результат новейших достижений биологии. Теперь известно, что живая клетка обязательно обладает двумя видами полимеров—белками и нуклеиновыми кислотами. В их взаимодействии заключены самые глубокие стороны явления жизни.
biofile.ru
|
Строительная: Белки участвуют в образовании клеточных и внеклеточных структур: входят в состав клеточных мембран (липопротеины, гликопротеины), волос (кератин), сухожилий (коллаген) и т.д. |
|
|
Транспортная: |
Белок крови гемоглобин присоединяет кислород и транспортирует его от легких ко всем тканям и органам, а от них в легкие переносит углекислый газ; в состав клеточных мембран входят особые белки, которые обеспечивают активный и строго избирательный перенос некоторых веществ и ионов из клетки во внешнюю среду и обратно. |
|
Регуляторная: Гормоны белковой природы принимают участие в регуляции процессов обмена веществ. Например, гормон инсулин регулирует уровень глюкозы в крови, способствует синтезу гликогена, увеличивает образование жиров из углеводов. |
|
|
Защитная: В ответ на проникновение в организм чужеродных белков или микроорганизмов (антигенов) образуются особые белки — антитела, способные связывать и обезвреживать их. Фибрин, образующийся из фибриногена, способствует остановке кровотечений. |
|
|
Двигательная: Сократительные белки актин и миозин обеспечивают сокращение мышц у многоклеточных животных. |
|
|
Сигнальная: В поверхностную мембрану клетки встроены молекулы белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды, таким образом осуществляя прием сигналов из внешней среды и передачу команд в клетку. |
|
|
Запасающая: В организме животных белки, как правило, не запасаются, исключение: альбумин яиц, казеин молока. Но благодаря белкам в организме могут откладываться про запас некоторые вещества, например, при распаде гемоглобина железо не выводится из организма, а сохраняется, образуя комплекс с белком ферритином. |
|
|
Энергетическая: При распаде 1 г белка до конечных продуктов выделяется 17,6 кДж. Сначала белки распадаются до аминокислот, а затем до конечных продуктов - воды, углекислого газа и аммиака. Однако в качестве источника энергии белки используются только тогда, когда другие источники (углеводы и жиры) израсходованы. |
|
|
Каталитическая: Одна из важнейших функций белков. Обеспечивается белками - ферментами, которые ускоряют биохимические реакции, происходящие в клетках. Например, рибулезобифосфаткарбоксилаза катализирует фиксацию СО2 при фотосинтезе. Copyright © BioFile 2007-2016 |
biofile.ru
Что такое белки, какой у них состав, зачем они нужны? :: SYL.ru
О том, что такое белки, сейчас знает практически каждый из школьных уроков биологии. Они выполняют множество функций в клетке живого существа.
Что такое белки?
Это сложные органические соединения. Они состоят из аминокислот, которых всего существует 20, однако, соединив их в разной последовательности, можно получить миллионы разнообразных химических веществ.
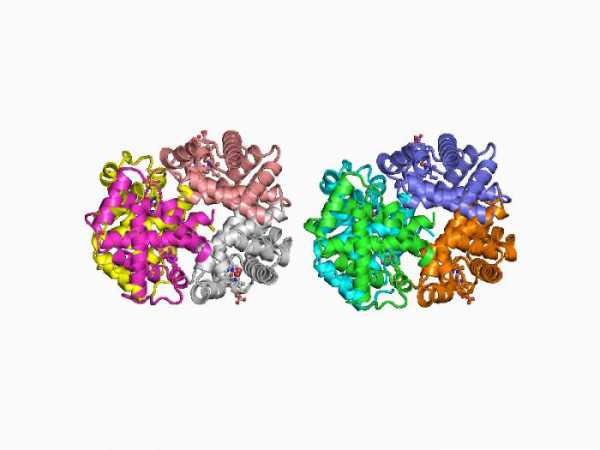
Структура белков
Когда мы уже знаем, что такое белки, можно подробнее рассмотреть их строение. Существует первичная, вторичная, третичная и четвертичная структура такого рода веществ.
Первичная структура
Это цепь, в которой аминокислоты соединены в нужном порядке. Это чередование и определяет вид белка. Для каждого вещества данного класса оно индивидуально. От первичной структуры во многом зависят также физические и химические свойства того или иного белка.
Вторичная структура
Это пространственная форма, которую принимает полипептидная цепь за счет образования водородных связей между карбоксильными группами и имино-группами. Существует два наиболее распространенных ее типа: альфа-спираль и бета-структура, имеющая лентообразный вид. Первая формируется вследствие возникновения связей между молекулами одной и той же полипептидной цепи, вторая — между двумя или более расположенными параллельно цепями. Однако также возможно возникновение бета-структуры и в пределах одного полимера — в том случае, когда определенные его фрагменты повернуты на 180 градусов.

Третичная структура
Это чередование и расположение относительно друг друга в пространстве участков альфа-спирали, простых полипептидных цепей и бета-структур.
Четвертичная структура
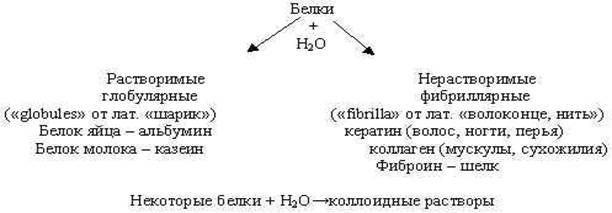
Ее также существует два вида: глобулярная и фибриллярная. Такая структура формируется за счет электростатических взаимодействий и водородных связей. Глобулярная имеет форму небольшого клубка, а фибриллярная — нити. Примерами белков с четвертичной структурой первого типа могут служить альбумин, инсулин, иммуноглобулин и т. д.; фибриллярных — фиброин, кератин, коллаген и другие. Есть и еще более сложные по строению белки, к примеру, миозин, содержащийся в мышечных тканях, он имеет стержень фибриллярной формы, на котором расположены две глобулярные головки.
Химический состав белков
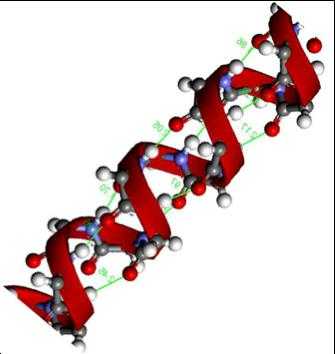
Аминокислотный состав белков может быть представлен двадцатью аминокислотами, которые комбинируются в различном порядке и количестве.
Это глицин, аланин, валин, лейцин, изолейцин, серин, треонин, цистеин, метионин, лизин, аргинин, аспарагиновая кислота, аспарагин, глутаминовая кислота, глутамин, фенилаланин, тирозин, триптофан, гистидин и пролин. Среди них есть незаменимые, то есть те, которые организм человека не в состоянии вырабатывать самостоятельно. Таких аминокислот насчитывается 8 для взрослых и еще 2 для детей: лейцин, изолейцин, валин, метионин, лизин, триптофан, фенилаланин, треонин, а также гистидин и аргинин.
Примеры белков с разной структурой
Ярким представителем глобулярных белков является альбумин. Его третичная структура состоит из альфа-спиралей, которые соединяются одиночными полипептидными цепочками.
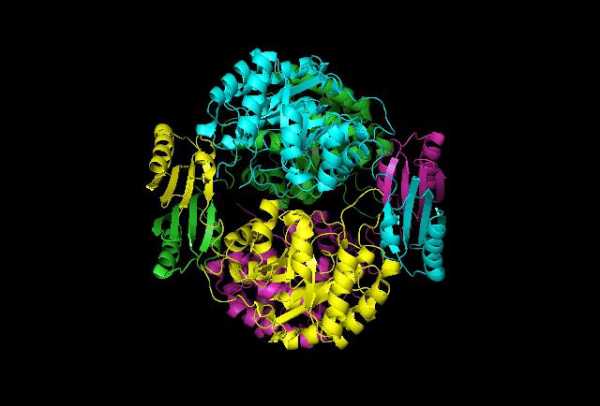
Первичная же образуется такими аминокислотами, как аспаргиновая кислота, аланин, цистеин и глицин. Данный белок находится в плазме крови и выполняет функцию транспорта определенных веществ. Из фибриллярных можно выделить фиброин и коллаген. Третичная структура первого представляет собой вещество из бета-структур, которые соединены одиночными полипептидными цепочками. Сама цепь представляет собой чередование аланина, глицина, цистеина и серина. Данное химическое соединение является основным компонентом паутины и шелка, а также перьев птиц.
Что такое денатурация?
Это процесс разрушения сперва четвертичной, затем третичной и вторичной структур белка. Белок, с которым это случилось, уже не может выполнять свои функции и теряет основные физические и химические свойства. Такой процесс происходит в основном из-за воздействия высоких температур или агрессивных химических веществ. К примеру, при температуре выше сорока градусов Цельсия начинает денатурировать гемоглобин, переносящий кислород по крови организмов. Вот почему для человека опасно столь сильное повышение температуры.

Функции белков
Узнав о том, что такое белки, можно обратить внимание на роль этих веществ в жизни клетки и всего организма в целом. Они выполняют девять основных функций. Первая — пластическая. Они являются компонентами многих структур живого организма и служат в качестве строительного материала для клетки. Вторая — транспортная. Белки способны переносить вещества, примером веществ данного назначения являются альбумин, гемоглобин, а также разнообразные белки-транспортеры, находящиеся на плазматической мембране клетки, каждый из которых пропускает только определенное вещество в цитоплазму из окружающей среды. Третья функция — защитная. Ее выполняют иммуноглобулины, которые являются частью иммунной системы, и коллаген, являющийся основным компонентом кожного покрова. Также белки в организме человека и других организмов выполняют регуляторную функцию, так как существует некоторое количество гормонов, представленных такого рода веществами, к примеру, как инсулин. Еще одна роль, выполняемая этими химическими соединениями, — сигнальная. Данные вещества передают электрические импульсы из клетки в клетку. Шестая функция — двигательная. Яркими представителями белков, выполняющих ее, являются актин и миозин, которые способны сокращаться (они находятся в мышцах). Такие вещества могут также служить запасными, однако в таких целях они используются довольно редко, в основном это белки, которые есть в молоке. Они выполняют еще и каталитическую функцию — в природе есть ферменты белковой природы. И последняя функция— рецепторная. Существует группа белков, которые частично денатурируют под воздействием того или иного фактора, давая таким образом сигнал всей клетке, которая передает его дальше.
www.syl.ru
Белки, их строение и роль в клетке | Биология. Реферат, доклад, сообщение, краткое содержание, конспект, сочинение, ГДЗ, тест, книга
Тема: Микробиология
Белки — основная структурная единица клеток. Это полимеры, мономерами которых являются аминокислоты. В состав белков входит 20 типов аминокислот. В каждой из аминокислот содержится аминогруппа (-NH), карбоксильная группа (-СООН) и радикал (R). Строение радикалов отличается у различных аминокислот. Соединение аминокислот в молекуле белка происходит благодаря образованию пептидной связи: аминогруппа одной аминокислоты соединяется с карбоксильной группой другой аминокислоты.
Соединение, состоящее из нескольких аминокислот, называют пептидом. Выделяют первичную, вторичную, третичную и четвертичную структуры белков. Первичная структура белка определяется последовательностью аминокислот в полипептидной цепи. Именно порядок чередования аминокислот в данной белковой молекуле определяет её особые физико-химические и биологические свойства.
Вторичная структура представляет собой белковую нить, закрученную в виде спирали. Между карбоксильными группами на одном витке спирали и аминогруппами на другом витке возникают водородные связи, которые слабее ковалентных, но при их большом числе обеспечивают образование прочной структуры.
Третичная структура — это клубок, или глобула, в который свертывается спираль. Он образуется в результате взаимодействия различных остатков аминокислот. Для каждого белка характерна своя форма.
Некоторые белки имеют четвертичную структуру. Она характерна для сложных белков. Несколько глобул объединены вместе и удерживаются вместе благодаря ионным, водородным и другим нековалентным связям. Например, белок гемоглобин — состоит из четырех глобул, каждая из которых соединена с железосодержащим гемом.
Под влиянием внешних факторов (изменение температуры, солевого состава среды, pH, под действием радиации и т.п. факторов) слабые химические связи, поддерживающие молекулу белка (вторичную, третичную, четвертичную структуры), разрываются, изменяются структура и свойства белка. Этот процесс называется денатурацией.
Роль белков: Материал с сайта //iEssay.ru
- Строительная функция. Белки входят в состав клеточных структур, являются структурными компонентами биологических мембран и многих внутриклеточных органоидов, главным компонентом опорных структур организма.
- Ферментативная функция. Многие белки служат биокатализаторами, ускоряют протекание различных химических реакций в организме.
- Регуляторная функция. Часть гормонов — белки. Они участвуют в регуляции активности клетки и организма. Например, инсулин регулирует обмен глюкозы.
- Защитная функция. Антитела, образуемые лимфоцитами, нейтрализуют чужеродных для организма возбудите лей заболеваний. Белки, участвующие в процессе свертывания крови (фибриноген и тромбин), предохраняют организм от кровопотери.
- Транспортная функция. Белки могут присоединять к себе различные молекулы и ионы и переносить их из одной части организма к другой. Например, гемоглобин переносит кислород и углекислый газ.
- Энергетическая функция. Белки могут служить источ ником энергии для клетки. При недостатке в организме yглеводов или жиров окисляются молекулы аминокислот. При расщеплении 1 г белков высвобождается 17,6 кДж энергии.
- белки характеристика
- биополимире белки их строение тест
iessay.ru
Строение белковБелки — высокомолекулярные органические соединения, состоящие из остатков α-аминокислот. В состав белков входят углерод, водород, азот, кислород, сера. Часть белков образует комплексы с другими молекулами, содержащими фосфор, железо, цинк и медь. Белки обладают большой молекулярной массой: яичный альбумин — 36 000, гемоглобин — 152 000, миозин — 500 000. Для сравнения: молекулярная масса спирта — 46, уксусной кислоты — 60, бензола — 78. Аминокислотный состав белковБелки — непериодические полимеры, мономерами которых являются α-аминокислоты. Обычно в качестве мономеров белков называют 20 видов α-аминокислот, хотя в клетках и тканях их обнаружено свыше 170. В зависимости от того, могут ли аминокислоты синтезироваться в организме человека и других животных, различают: заменимые аминокислоты — могут синтезироваться; незаменимые аминокислоты — не могут синтезироваться. Незаменимые аминокислоты должны поступать в организм вместе с пищей. Растения синтезируют все виды аминокислот. В зависимости от аминокислотного состава, белки бывают: полноценными — содержат весь набор аминокислот;неполноценными — какие-то аминокислоты в их составе отсутствуют. Если белки состоят только из аминокислот, их называютпростыми. Если белки содержат помимо аминокислот еще и неаминокислотный компонент (простетическую группу), их называютсложными. Простетическая группа может быть представлена металлами (металлопротеины), углеводами (гликопротеины), липидами (липопротеины), нуклеиновыми кислотами (нуклеопротеины). Все аминокислоты содержат: 1) карбоксильную группу (–СООН), 2) аминогруппу (–NH2), 3) радикал или R-группу (остальная часть молекулы). Строение радикала у разных видов аминокислот — различное. В зависимости от количества аминогрупп и карбоксильных групп, входящих в состав аминокислот, различают:нейтральные аминокислоты, имеющие одну карбоксильную группу и одну аминогруппу; основные аминокислоты, имеющие более одной аминогруппы; кислые аминокислоты, имеющие более одной карбоксильной группы. Аминокислоты являются амфотерными соединениями, так как в растворе они могут выступать как в роли кислот, так и оснований. В водных растворах аминокислоты существуют в разных ионных формах. Пептидная связьПептиды — органические вещества, состоящие из остатков аминокислот, соединенных пептидной связью. Образование пептидов происходит в результате реакции конденсации аминокислот. При взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой между ними возникает ковалентная азот-углеродная связь, которую и называютпептидной. В зависимости от количества аминокислотных остатков, входящих в состав пептида, различают дипептиды, трипептиды, тетрапептиды и т.д. Образование пептидной связи может повторяться многократно. Это приводит к образованиюполипептидов. На одном конце пептида находится свободная аминогруппа (его называют N-концом), а на другом — свободная карбоксильная группа (его называют С-концом). Пространственная организация белковых молекулВыполнение белками определенных специфических функций зависит от пространственной конфигурации их молекул, кроме того, клетке энергетически невыгодно держать белки в развернутой форме, в виде цепочки, поэтому полипептидные цепи подвергаются укладке, приобретая определенную трехмерную структуру, или конформацию. Выделяют 4 уровня пространственной организации белков. Первичная структура белка — последовательность расположения аминокислотных остатков в полипептидной цепи, составляющей молекулу белка. Связь между аминокислотами — пептидная. Если молекула белка состоит всего из 10 аминокислотных остатков, то число теоретически возможных вариантов белковых молекул, отличающихся порядком чередования аминокислот, — 1020. Имея 20 аминокислот, можно составить из них еще большее количество разнообразных комбинаций. В организме человека обнаружено порядка десяти тысяч различных белков, которые отличаются как друг от друга, так и от белков других организмов. Именно первичная структура белковой молекулы определяет свойства молекул белка и ее пространственную конфигурацию. Замена всего лишь одной аминокислоты на другую в полипептидной цепочке приводит к изменению свойств и функций белка. Например, замена в β-субъединице гемоглобина шестой глутаминовой аминокислоты на валин приводит к тому, что молекула гемоглобина в целом не может выполнять свою основную функцию — транспорт кислорода; в таких случаях у человека развивается заболевание — серповидноклеточная анемия. Вторичная структура — упорядоченное свертывание полипептидной цепи в спираль (имеет вид растянутой пружины). Витки спирали укрепляются водородными связями, возникающими между карбоксильными группами и аминогруппами. Практически все СО- и NН-группы принимают участие в образовании водородных связей. Они слабее пептидных, но, повторяясь многократно, придают данной конфигурации устойчивость и жесткость. На уровне вторичной структуры существуют белки: фиброин (шелк, паутина), кератин (волосы, ногти), коллаген (сухожилия). Третичная структура — укладка полипептидных цепей в глобулы, возникающая в результате возникновения химических связей (водородных, ионных, дисульфидных) и установления гидрофобных взаимодействий между радикалами аминокислотных остатков. Основную роль в образовании третичной структуры играют гидрофильно-гидрофобные взаимодействия. В водных растворах гидрофобные радикалы стремятся спрятаться от воды, группируясь внутри глобулы, в то время как гидрофильные радикалы в результате гидратации (взаимодействия с диполями воды) стремятся оказаться на поверхности молекулы. У некоторых белков третичная структура стабилизируется дисульфидными ковалентными связями, возникающими между атомами серы двух остатков цистеина. На уровне третичной структуры существуют ферменты, антитела, некоторые гормоны. 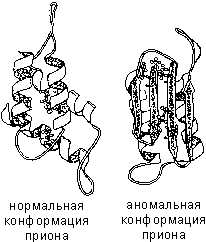 Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами. Субъединицы удерживаются в молекуле благодаря ионным, гидрофобным и электростатическим взаимодействиям. Иногда при образовании четвертичной структуры между субъединицами возникают дисульфидные связи. Наиболее изученным белком, имеющим четвертичную структуру, является гемоглобин. Он образован двумя α-субъединицами (141 аминокислотный остаток) и двумя β-субъединицами (146 аминокислотных остатков). С каждой субъединицей связана молекула гема, содержащая железо. Если по каким-либо причинам пространственная конформация белков отклоняется от нормальной, белок не может выполнять свои функции. Например, причиной «коровьего бешенства» (губкообразной энцефалопатии) является аномальная конформация прионов — поверхностных белков нервных клеток. Свойства белковАминокислотный состав, структура белковой молекулы определяют его свойства. Белки сочетают в себе основные и кислотные свойства, определяемые радикалами аминокислот: чем больше кислых аминокислот в белке, тем ярче выражены его кислотные свойства. Способность отдавать и присоединять Н+ определяют буферные свойства белков; один из самых мощных буферов — гемоглобин в эритроцитах, поддерживающий рН крови на постоянном уровне. Есть белки растворимые (фибриноген), есть нерастворимые, выполняющие механические функции (фиброин, кератин, коллаген). Есть белки активные в химическом отношении (ферменты), есть химически неактивные, устойчивые к воздействию различных условий внешней среды и крайне неустойчивые. Внешние факторы (нагревание, ультрафиолетовое излучение, тяжелые металлы и их соли, изменения рН, радиация, обезвоживание) могут вызывать нарушение структурной организации молекулы белка. Процесс утраты трехмерной конформации, присущей данной молекуле белка, называют денатурацией. Причиной денатурации является разрыв связей, стабилизирующих определенную структуру белка. Первоначально рвутся наиболее слабые связи, а при ужесточении условий и более сильные. Поэтому сначала утрачивается четвертичная, затем третичная и вторичная структуры. Изменение пространственной конфигурации приводит к изменению свойств белка и, как следствие, делает невозможным выполнение белком свойственных ему биологических функций. Если денатурация не сопровождается разрушением первичной структуры, то она может быть обратимой, в этом случае происходит самовосстановление свойственной белку конформации. Такой денатурации подвергаются, например, рецепторные белки мембраны. Процесс восстановления структуры белка после денатурации называется ренатурацией. Если восстановление пространственной конфигурации белка невозможно, то денатурация называется необратимой. Функции белков
ФерментыФерменты, или энзимы, — особый класс белков, являющихся биологическими катализаторами. Благодаря ферментам биохимические реакции протекают с огромной скоростью. Скорость ферментативных реакций в десятки тысяч раз (а иногда и в миллионы) выше скорости реакций, идущих с участием неорганических катализаторов. Вещество, на которое оказывает свое действие фермент, называют субстратом. Ферменты — глобулярные белки, по особенностям строения ферменты можно разделить на две группы: простые и сложные.Простые ферменты являются простыми белками, т.е. состоят только из аминокислот. Сложные ферменты являются сложными белками, т.е. в их состав помимо белковой части входит группа небелковой природы — кофактор. У некоторых ферментов в качестве кофакторов выступают витамины. В молекуле фермента выделяют особую часть, называемую активным центром.Активный центр — небольшой участок фермента (от трех до двенадцати аминокислотных остатков), где и происходит связывание субстрата или субстратов с образованием фермент-субстратного комплекса. По завершении реакции фермент-субстратный комплекс распадается на фермент и продукт (продукты) реакции. Некоторые ферменты имеют (кроме активного)аллостерические центры — участки, к которым присоединяются регуляторы скорости работы фермента (аллостерические ферменты). 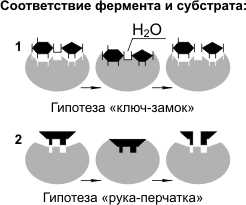 Для реакций ферментативного катализа характерны: 1) высокая эффективность, 2) строгая избирательность и направленность действия, 3) субстратная специфичность, 4) тонкая и точная регуляция. Субстратную и реакционную специфичность реакций ферментативного катализа объясняют гипотезы Э. Фишера (1890 г.) и Д. Кошланда (1959 г.). Э. Фишер (гипотеза «ключ-замок») предположил, что пространственные конфигурации активного центра фермента и субстрата должны точно соответствовать друг другу. Субстрат сравнивается с «ключом», фермент — с «замком». Д. Кошланд (гипотеза «рука-перчатка») предположил, что пространственное соответствие структуры субстрата и активного центра фермента создается лишь в момент их взаимодействия друг с другом. Эту гипотезу еще называют гипотезой индуцированного соответствия. Скорость ферментативных реакций зависит от: 1) температуры, 2) концентрации фермента, 3) концентрации субстрата, 4) рН. Следует подчеркнуть, что поскольку ферменты являются белками, то их активность наиболее высока при физиологически нормальных условиях. Большинство ферментов может работать только при температуре от 0 до 40 °С. В этих пределах скорость реакции повышается примерно в 2 раза при повышении температуры на каждые 10 °С. При температуре выше 40 °С белок подвергается денатурации и активность фермента падает. При температуре, близкой к точке замерзания, ферменты инактивируются. При увеличении количества субстрата скорость ферментативной реакции растет до тех пор, пока количество молекул субстрата не станет равным количеству молекул фермента. При дальнейшем увеличении количества субстрата скорость увеличиваться не будет, так как происходит насыщение активных центров фермента. Увеличение концентрации фермента приводит к усилению каталитической активности, так как в единицу времени преобразованиям подвергается большее количество молекул субстрата. Для каждого фермента существует оптимальное значение рН, при котором он проявляет максимальную активность (пепсин — 2,0, амилаза слюны — 6,8, липаза поджелудочной железы — 9,0). При более высоких или низких значениях рН активность фермента снижается. При резких сдвигах рН фермент денатурирует. Скорость работы аллостерических ферментов регулируется веществами, присоединяющимися к аллостерическим центрам. Если эти вещества ускоряют реакцию, они называются активаторами, если тормозят — ингибиторами. Классификация ферментовПо типу катализируемых химических превращений ферменты разделены на 6 классов:
Классы в свою очередь подразделены на подклассы и подподклассы. В действующей международной классификации каждый фермент имеет определенный шифр, состоящий из четырех чисел, разделенных точками. Первое число — класс, второе — подкласс, третье — подподкласс, четвертое — порядковый номер фермента в данном подподклассе, например, шифр аргиназы — 3.5.3.1. |
lidijavk.ucoz.ru
Белки
Человеческий организм состоит из ста триллионов клеток, каждая клетка состоит из сотен миллионов молекул белка. Белки ─ это строительные материалы и живые нано-машины нашего тела.
По сравнению с липидами и углеводами белки являются наиболее важными для организма.
Каждый из сотен тысяч разных белков обладает неповторимой пространственной структурой. И у каждого белка своя задача и функция. Есть белки костной и мышечной ткани, белки тканей кожи и мозга. Белки ферменты и рецепторы.
Если в организме отсутствует хотя бы один белок (например, белковый гормон инсулин) жизнь человека в опасности, так как инсулин оказывает многогранное влияние на обмен практически во всех тканях.
Основное действие инсулина заключается в снижении концентрации глюкозы в крови.
Белки — это самые сложные молекулярные системы, имеющиеся в природе.
Кроме углерода, кислорода, водорода и азота в состав белков могут входить сера, фосфор, железо.
Белки построены из мономеров, которыми являются аминокислоты.
Среди двухсот известных аминокислот только 20 из них участвуют во внутриклеточном синтезе белков. Их называют протеиногенными или стандартными аминокислотами. Вопрос, почему именно эти 20 аминокислот стали «избранными», остаётся нерешённым. Не совсем ясно, чем эти аминокислоты оказались предпочтительнее других похожих.
Из 20 аминокислот, входящих в состав белков, может быть образовано вот такое число комбинаций различных белков, которые будут обладать совершенно одинаковым составом, но различным строением.
Все аминокислоты подразделяют на заменимые и незаменимые.
Заменимые аминокислоты синтезируются в организме человека, к ним относят: аланин, аргинин, аспарагин, аспарагиновую кислоту, глицин, глутамин, глутаминовую кислоту, пролин, серин, тирозин и цистеин.
Незаменимые аминокислоты в организме не синтезируются и должны в обязательном порядке поступать с пищей. Это валин, гистидин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин. Содержатся они в основном в продуктах животного происхождения.
Для удобства названия аминокислот имеют общепринятые сокращения.
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (─Nh4), с основными свойствами, другая – карбоксильной группой (─COOH) с кислотными свойствами.
Часть молекулы, которая называется радикалом (в формулах она обычно обозначается большой латинской буквой эр R), у разных аминокислот имеет различное строение.
Аминокислоты соединяются между собой. Так образуется молекула, которая представляет собой пептид. Эта реакция называется (полимеризацией).
В процессе полимеризации выделяется молекула воды, а освободившиеся электроны образуют ковалентную связь, которая получила название пептидной. Это связь между атомами углерода и азота.
Поскольку на одном конце дипептида находится свободная аминогруппа, а на другом – свободная карбоксильная группа, дипептид может присоединять к себе другие аминокислоты.
Также белки могут состоять и из большого числа аминокислотных остатков. И кроме того каждая аминокислота может встречаться в белке несколько раз.
В состав белка может входить одна, две и более полипептидные цепи. Например, в молекуле инсулина – две цепи, а иммуноглобулины состоят из четырёх цепей.
Среди белков различают протеины, состоящие только из белков и протеиды, содержащие не белковую часть. Например, гемоглобин.
Гемоглобин является сложным белком класса хромопротеинов, то есть в качестве небелкового компонента здесь выступает особая пигментная группа, содержащая железо, — гем.
Гемоглобин человека является тетрамером, то есть состоит из четырёх субъединиц. У взрослого человека они представлены полипептидными цепями α1 (альфа-1), α2, β1(бета-1) и β2.
Четвертичная структура гемоглобина придаёт ему способность регулировать присоединение и отщепление кислорода.
Гемоглобин является одним из основных белков, которыми питаются малярийные плазмодии — возбудители малярии. В эндемичных по малярии районах земного шара весьма распространены наследственные аномалии строения гемоглобина.
Эритроцит при этом приобретает форму серпа. Из-за этого малярийный плазмодий не проникает в эритроцит и не питается белком-гемоглобином. Изменение в форме эритроцита приводит к заболеванию серповидноклеточной анемии.
Если белки состоят только из аминокислот, то их называют простыми.
Если в состав белков входят компоненты неаминокислотной природы, то такие белки относят к сложным.
Если в состав сложных белков входят углеводы, то их называют гликопротеиды. Если входят жиры – то липопротеиды, а если нуклеиновые кислоты – нуклеопротеиды.
Именно строение белковых молекул определяет многообразие функций белков и их особую роль в жизненных процессах. Поэтому исследование структуры белков ─ самая важная стадия познания явлений, происходящих в живой клетке.
Попытаемся обнаружить белок, выявить его присутствие.
Белок можно выявить при помощи его денатурации.
Денатурация — это утрата белковой молекулой своей первоначальной структуры.
Денатурация может возникать под воздействием нагревания (температуры), химических веществ (например, кислот, оснований, органических растворителей), обезвоживания, облучения и других факторов, в результате которых свойство белковых молекул резко изменяется.
Зажигаем спиртовку, наливаем в демонстрационную пробирку каллоидный раствор белка в дистиллированной воде. Закрепляем пробирку в держалке и осторожно нагреваем содержимое пробирки. Уже при небольшом нагревании хорошо видны изменения, происходящие в растворе. Он перестаёт быть прозрачным, появляется белый осадок. Это и есть свернувшийся белок. Температура (нагревание) вызывает свёртывание коллоидного раствора белка.
Следующий опыт
В пробирку с коллоидным раствором белка в дистиллированной воде добавляем разбавленный раствор азотной кислоты. Признак реакции ─ образование осадка. Белок денатурирован.
Третий опыт
Денатурация белка происходит и под действием растворов солей тяжёлых метоллов. К раствору белка добавляем раствор сульфата меди. Признаком реакции является образование белого непрозрачного осадка. Это и есть денатурированный белок.
Обнаружив белок, мы ничего не можем сказать о его составе, структуре, свойствах. Что бы ответить на все эти вопросы необходимо, пряже всего, выделить белок — получить его в чистом виде. Существует множество методов получения белков в чистом виде.
Процесс, обратный денатурации, при котором белки возвращают свою природную структуру, называется ренатурацией.
Уровни организации белковой молекулы
Молекулы белков могут принимать различные пространственные формы – конформации, которые представляют собой четыре уровня их организации.
Последовательное чередование различных аминокислотных звеньев в полипептидной цепи называется – первичной структурой белковой молекулы. Она уникальна для любого белка и определяет его форму, свойства и функции.
Молекула белка обладает определённой пространственной формой – это вторичная структура. Такая структура поддерживается водородными связями. Водородные связи возникают межу амино- и карбоксильными группами амикислотных остатков полипептидной цепи.
Водородные связи фиксируют различные пространственные структуры. Хотя они и малопрочные, но из-за того, что их большое количество, – вторичная структура белка достаточно прочна.
Части белковой молекулы могут организовываться в спираль или в другие виды вторичной структуры.
Третичная структура белка имеет вид клубка (глобулы). Третичная структура — это трёхмерная организация белковой молекулы. Она поддерживается водородными и дисульфидными (-S-S-) связями между остатками цисцеина (аминокислоты), а также гидрофобными взаимодействиями.
Существует и четвертичная структура белка. Однако она характерна не для всех молекул белка. Четвертичная структура возникает в результате соединения нескольких глобул в сложный комплекс. Например, гемоглобин крови состоит из четырёх таких субъединиц.
Как вы уже поняли, белки многочисленны и многообразны. И у каждого белка своя задача и функция.
Рассмотрим некоторые из них.
Структурная функция белков. Так как белки являются основой всех биологических мембран, они выполняют строительную функцию.
Белок коллаген — важный составной компонент соединительных тканей.
Эластин — эластичный компонент связок, стенок кровеносных сосудов.
Кератин — фибриллярный белок, обладающий механической прочностью, которая среди материалов биологического происхождения уступает лишь хитину. В основном из кератинов состоят роговые производные эпидермиса кожи — такие структуры, как волосы, ногти, рога, перья и роговой чехол, который покрывает клюв птиц.
Ферментативная функция белков.
Ферменты — вещества белковой природы. Их молекулы состоят в основном из аминокислотных звеньев.
Ферменты специфичны для каждого вещества. Основная функция их — это ускорение биохимических реакций организма, реакций распада и синтеза.
Они действуют в строго определённой последовательности.
Почему так? Дело в том, что избирательность действия ферментов на разные химические вещества связана с их строением. Ферменты имеют специфические активные участки (центры), с которыми связываются субстраты.
Форма и химическое строение активного центра таково, что с ним могут связаться только определённые молекулы в силу их пространственного соответствия, они подходят друг к другу, как ключ к замку. Связывание субстрата осуществляется именно в активном центре фермента.
Одни ферментные системы направляют процессы биосинтеза. Этот процесс требует затрат энергии.
Другие ферментные системы регулируют распад и окисление веществ. При этих реакциях энергия выделяется.
На заключительном этапе химической реакции комплекс распадается с образованием конечных продуктов и свободного фермента.
Освободившийся при этом активный центр фермента может снова принимать новые молекулы вещества – субстрата.
Многие ферменты как мы уже сказали представлены белковыми молекулами. Другие состоят не только из белка, но и из небелкового соединения (кофермента). В качестве кофермента могут выступать различные вещества, но, как правило, это витамины и ионы металлов.
Отсутствие витамина в пище сначала приводит к недостаточному образованию кофермента, а без него не может работать (активироваться) соответствующий фермент. Поэтому скорость биохимической реакции, за которую отвечает этот фермент, значительно падает. Итогом этого становится нарушение обмена веществ.
Транспортная функция белков имеет важное значение. Так, гемоглобин переносит кислород из лёгких к клеткам других тканей.
В мышцах эту функцию выполняет белок миоглобин.
Сывороточный альбумин крови способствует переносу липидов и жирных кислот, различных биологически активных веществ.
Белки-переносчики осуществляют перенос веществ через клеточные мембраны.
Специфические белки выполняют защитную функцию. Они предохраняют организм от вторжения чужеродных организмов и от повреждения.
Например, на проникновение в организм чужеродных белков реагирует иммунная система организма. Она бросает против них целую армию своих белков, так называемых антител.
Антитела являются особым классом гликопротеинов, имеющихся на поверхности B-лимфоцитов в виде мембраносвязанных рецепторов.
При помощи антиген-связывающих участков антитела присоединяются к вирусам и бактериям, чужеродным белкам, препятствуя их размножению.
Ещё один важный белок нашего организма — интерферон, — универсальный противовирусный белок.
Фибриноген и тромбин предохраняют организм от кровопотери, образуя тромб.
Многие живые существа для обеспечения защиты выделяют белки, называемые токсинами, которые в большинстве случаев являются сильными ядами.
Регуляторная функция белков
Она присуща белкам-гормонам (регуляторам). Они регулируют различные физиологические процессы.
Например, наиболее известным гормоном является упомянутый выше инсулин, регулирующий содержание глюкозы в крови. При недостатке инсулина в организме возникает заболевание, известное как сахарный диабет.
Белки могут выполнять энергетическую функцию, являясь одним из источников энергии в клетке. При полном расщеплении 1 г белка до конечных продуктов выделяется 17,6 кДж энергии.
Но в качестве источника энергии белки используются в последнюю очередь, после углеводов и жиров. Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Таким образом роль белков огромна. Современная биология показала, что сходство и различие организмов определяются в конечном счёте набором белков. Чем ближе организмы друг к другу в систематическом положении, тем более сходны их белки.
videouroki.net