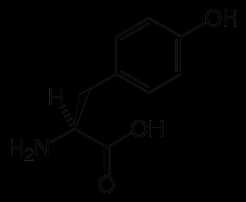
Формула Тирозина структурная химическая
Структурная формула
 |
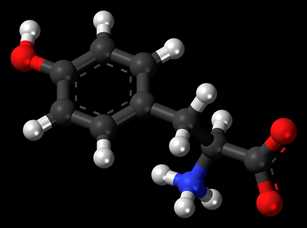 |
Истинная, эмпирическая, или брутто-формула: C9H11NO3
Химический состав Тирозина
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| C | Углерод | 12,011 | 9 | 59,7% |
| H | Водород | 1,008 | 11 | 6,1% |
| N | Азот | 14,007 | 1 | 7,7% |
| O | Кислород | 15,999 | 3 | 26,5% |
Молекулярная масса: 181,19
Тирози́н(α-амино-β-(п-гидроксифенил)пропионовая кислота, сокр.: Тир, Tyr, Y) — ароматическая альфа-аминокислота. Существует в двух оптически изомерных формах — L и D и в виде рацемата (DL). По строению соединение отличается от фенилаланина наличием фенольной гидроксильной группы в пара-положении бензольного кольца. Известны менее важные с биологической точки зрения мета- и орто- изомеры тирозина. L-тирозин является протеиногенной аминокислотой и входит в состав белков всех известных живых организмов. Тирозин входит в состав ферментов, во многих из которых именно тирозину отведена ключевая роль в ферментативной активности и её регуляции. Местом атаки фосфорилирующих ферментов протеинкиназ часто является именно фенольный гидроксил остатков тирозина. Остаток тирозина в составе белков может подвергаться и другим посттрансляционным модификациям. В некоторых белках (резилин насекомых) присутствуют молекулярные сшивки, возникающие в результате посттрансляционной окислительной конденсации остатков тирозина с образованием дитирозина и тритирозина. Окрашивание в результате ксантопротеиновой качественной реакции на белки определяется преимущественно нитрованием остатков тирозина (нитруются также остатки фенилаланина, триптофана, и гистидина).
Биосинтез
В процессе биосинтеза тирозина промежуточными соединениями являются шикимат, хоризмат, префенат. Из центральных метаболитов тирозин в природе синтезируют микроорганизмы, грибы и растения. Животные не синтезируют тирозин de novo, но способны гидроксилировать незаменимую аминокислоту фенилаланин в тирозин. Более подробно биосинтез тирозина рассмотрен в статье шикиматный путь. Тирозин относят к заменимым для большинства животных и человека аминокислотам, так как в организме эта аминокислота образуется из другой (незаменимой) аминокислоты — фенилаланина.
Катаболизм
В организм животных и человека тирозин поступает с пищей. Также тирозин образуется из фенилаланина (реакция протекает в печени под действием фермента фенилаланин-4-гидроксилазы). Превращение фенилаланина в тирозин в организме в большей степени необходимо для удаления избытка фенилаланина, а не для восстановления запасов тирозина, так как тирозин обычно в достаточном количестве поступает с белками пищи, и его дефицита, как правило, не возникает. Избыток тирозина утилизируется. Тирозин путём переаминирования с α-кетоглутаровой кислотой превращается в 4-гидроксифенилпируват, который далее окисляется (с одновременной миграцией и декарбоксилированием кетокарбоксиэтильного заместителя) в гомогентизат. Гомогентизат через стадии образования 4-малеилацетоацетата и 4-фумарилацетоацетата распадается до фумарата и ацетоацетата. Окончательное разрушение происходит в цикле Кребса. Таким образом, у животных и человека тирозин распадаются до фумарата (превращается в оксалоацетат, являющийся субстратом глюконеогенеза) и ацетоацетата (повышает уровень кетоновых тел в крови), поэтому тирозин, а также превращающийся в него фенилаланин, по характеру катаболизма у животных относят к глюко-кетогенным (смешанным) аминокислотам. В природе известны и другие пути биодеградации тирозина. Из тирозина синтезируются такие биологически активные вещества, как ДОФА, тиреоидные гормоны (тироксин, трийодтиронин). ДОФА является предшественником катехоламинов (дофамин, адреналин, норадреналин) и пигмента меланина. Гомогентизат является предшественником токоферолов, пластохинона (у организмов, способных синтезировать эти соединения). С обменом тирозина связаны некоторые известные наследственные заболевания. При наследственном заболевании фенилкетонурии превращение фенилаланина в тирозин нарушено, и в организме происходит накопление фенилаланина и его метаболитов (фенилпируват, фениллактат, фенилацетат, орто-гидроксифенилацетат, фенилацетилглутамин), избыточное количество которых отрицательно сказывается на развитии нервной системы. При другом известном наследственном заболевании — алкаптонурии — нарушено превращение гомогентизата в 4-малеилацетоацетат. Известно также несколько относительно редких заболеваний (тирозинемии), вызванных нарушениями обмена тирозина. Лечение этих заболеваний, как и фенилкетонурии — диетическое ограничение белка.
Применение
Тирозин подавляет аппетит, способствует уменьшению отложения жиров, способствует выработке меланина и улучшает функции надпочечников, щитовидной железы и гипофиза.
formula-info.ru
Тирозин — Википедия. Что такое Тирозин
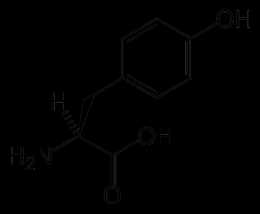
| Тирозин | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | 2-амино-3-(4- гидроксифенил) пропановая кислота |
| Сокращения | Тир, Tyr, Y UAU,UAC |
| Хим. формула | C₉H₁₁NO₃ |
| Рац. формула | C9H11NO3 |
| Физические свойства | |
| Молярная масса | 181,19 г/моль |
| Плотность | 1,456 г/см³ |
| Термические свойства | |
| Т. плав. | 343 °C |
| Химические свойства | |
| pKa | 2,24 9,04 10,10 |
| Рег. номер CAS | [60-18-4] |
| PubChem | 6057 |
| Рег. номер EINECS | 200—460-4 |
| SMILES | |
| InChI | |
| ChEBI | 17895 и 46161 |
| ChemSpider | 5833 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Тирози́н (α-амино-β-(п-гидроксифенил)пропионовая кислота, сокр.: Тир, Tyr, Y) — ароматическая альфа-аминокислота. Существует в двух оптически изомерных формах — L и D и в виде рацемата (DL). По строению соединение отличается от фенилаланина наличием фенольной гидроксильной группы в пара-положении бензольного кольца. Известны менее важные с биологической точки зрения
L-тирозин является протеиногенной аминокислотой и входит в состав белков всех известных живых организмов. Тирозин входит в состав ферментов, во многих из которых именно тирозину отведена ключевая роль в ферментативной активности и её регуляции. Местом атаки фосфорилирующих ферментов протеинкиназ часто является именно фенольный гидроксил остатков тирозина. Остаток тирозина в составе белков может подвергаться и другим посттрансляционным модификациям. В некоторых белках (резилин насекомых) присутствуют молекулярные сшивки, возникающие в результате посттрансляционной окислительной конденсации остатков тирозина с образованием дитирозина и тритирозина.
Окрашивание в результате ксантопротеиновой качественной реакции на белки определяется преимущественно нитрованием остатков тирозина (нитруются также остатки фенилаланина, триптофана, и гистидина).
Биосинтез
В процессе биосинтеза тирозина промежуточными соединениями являются шикимат, хоризмат, префенат. Из центральных метаболитов тирозин в природе синтезируют микроорганизмы, грибы и растения. Животные не синтезируют тирозин de novo, но способны гидроксилировать незаменимую аминокислоту фенилаланин в тирозин. Более подробно биосинтез тирозина рассмотрен в статье шикиматный путь.
Тирозин относят к
Катаболизм
В организм животных и человека тирозин поступает с пищей. Также тирозин образуется из фенилаланина (реакция протекает в печени под действием фермента фенилаланин-4-гидроксилазы). Превращение фенилаланина в тирозин в организме в большей степени необходимо для удаления избытка фенилаланина, а не для восстановления запасов тирозина, так как тирозин обычно в достаточном количестве поступает с белками пищи, и его дефицита, как правило, не возникает. Избыток тирозина утилизируется. Тирозин путём переаминирования с α-кетоглутаровой кислотой превращается в 4-гидроксифенилпируват, который далее окисляется (с одновременной миграцией и декарбоксилированием кетокарбоксиэтильного заместителя) в гомогентизат. Гомогентизат через стадии образования 4-малеилацетоацетата и 4-фумарилацетоацетата распадается до фумарата и ацетоацетата. Окончательное разрушение происходит в цикле Кребса.
Таким образом, у животных и человека тирозин распадаются до фумарата (превращается в оксалоацетат, являющийся субстратом глюконеогенеза) и ацетоацетата (повышает уровень кетоновых тел в крови), поэтому тирозин, а также превращающийся в него фенилаланин, по характеру катаболизма у животных относят к глюко-кетогенным (смешанным) аминокислотам (см. классификацию аминокислот).
В природе известны и другие пути биодеградации тирозина.
Из тирозина синтезируются такие биологически активные вещества, как ДОФА, тиреоидных гормонов (тироксин, трийодтиронин). ДОФА является предшественником катехоламинов (дофамин, адреналин, норадреналин) и пигмента меланина. Гомогентизат является предшественником токоферолов, пластохинона (у организмов, способных синтезировать эти соединения).
С обменом тирозина связаны некоторые известные наследственные заболевания. При наследственном заболевании фенилкетонурии превращение фенилаланина в тирозин нарушено, и в организме происходит накопление фенилаланина и его метаболитов (фенилпируват, фениллактат, фенилацетат, орто-гидроксифенилацетат, фенилацетилглутамин), избыточное количество которых отрицательно сказывается на развитии нервной системы. При другом известном наследственном заболевании — алкаптонурии — нарушено превращение гомогентизата в 4-малеилацетоацетат.
Известно также несколько относительно редких заболеваний (тирозинемии), вызванных нарушениями обмена тирозина. Лечение этих заболеваний, как и фенилкетонурии — диетическое ограничение белка.
Применение
Тирозин подавляет аппетит, способствует уменьшению отложения жиров, способствует выработке меланина и улучшает функции надпочечников, щитовидной железы и гипофиза.[источник не указан 2935 дней]
См. также
Литература
- Report of Medical Research Council on the Dietary Management of PKU. Recommendations on the Dietary Management of PKU. Arch. Dis. Child. 1993: 68; 426-7.
- Dixon M., MacDonald A, White F. Disorders of Amino Acid Metabolism, Organic Acidemias and Urea Cycle Defects PKU in Lawson M, Shaw V (eds.). Clinical Paediatric Dietetics. Oxford:Blackwell Science, 2001,p233-294.
- Holme E, Linstedt S. Tyrosinemia Type I adn NTBC (2-(2-nitro-4-triflourom othylbenoyl)-1,3-cyclohexanedione). J. Inherit. Metab. Dis. 1998:21;507-517.
- Ellaway CJ., Holme E, Standing S. et al. Outcome of Tyrosinemia Type III. J. Inherit. Metab. Dis 2001:24;824-32.
wiki.sc
тирозин — полезные свойства и инструкция по применению
Содержание статьи:
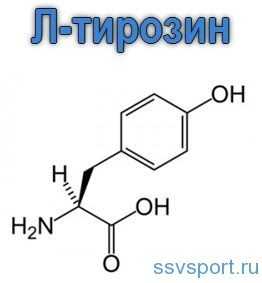 Л-тирозин – это аминокислота, которая присутствует в каждой клетке организма человека. Она играет немаловажную роль в синтезировании белка и гормонов, участвует в производстве нейромедиаторов.
Л-тирозин – это аминокислота, которая присутствует в каждой клетке организма человека. Она играет немаловажную роль в синтезировании белка и гормонов, участвует в производстве нейромедиаторов.
Биологические добавки с тирозином способствуют повышению настроения, улучшению памяти, снижению волнений и рассеянности и стабилизируют общий эмоциональный фон.
Организм человека самостоятельно вырабатывает Л-тирозин в необходимом количестве, поэтому он относится к числу заменимых аминокислот. Кроме того, это вещество содержится во многих белковых продуктах питания.
Описание товара. Рекомендации по применению. Отзывы. Подробнее >>
Благодаря биодобавкам с Л-тирозином возможно лечение депрессии и психоза. Регулярное применение таких препаратов избавляет от заторможенности, восстанавливает процессы, нарушенные психическим расстройством.
Рассмотрим, каковы полезные свойства тирозина, каких случаях назначают препарат Л тирозин, как его принимать, существуют ли противопоказания к приёму этой аминокислоты. Также в этой статье вы найдете отзывы о применении добавок с тирозином и где купить Л тирозин.
Л-тирозин полезные свойства аминокислоты
Слово «тирозин» происходит от греческого «тири» и обозначает в переводе «сыр». Эта аминокислота была обнаружена немецким ученым Либихом в казеине протеине, который содержится в сыре — отсюда и название.
Существует три формы тирозина: L-тирозин аминокислота, находящаяся в белках организмов; D-тирозин нейромедиатор, находящийся в ферментах; DL тирозин, не обладающий оптической энергией.
Химическое название аминокислоты 4-гидроксифенилаланин. Благодаря тирозину протекают различные биологические процессы организма и активируется распад белковых компонентов, входящих в различные клеточные структуры и ферменты. Кроме того, он играет важную роль в синтезе таких гормонов, как дофамин, адреналин, норадреналин, тироксин.
Как Л-Тирозин влияет на отдельные системы:
- Неврология. Профилактика развития постстрессовой амнезии. Снижается сонливость и улучшается концентрация внимания. Вырабатываются гормоны катехоламины в крови как защитная реакция на сильную стимуляцию стрессом нервной системы. Уменьшается агрессивность, напряжение и раздраженность во время стрессов.
- Сердечно-сосудистая система. Нормализуется систолическое и диастолическое артериальное давление на фоне гипертонии. Лечение вегето-сосудистой дистонии.
- Похудение. Л-тирозин помогает в похудении за счет усиления обмена веществ, а также он оказывает жиросжигающий эффект.
- Заболевания. Лечение болезни Паркинсона в комплексе с другими лечебными препаратами. Повышение либидо (сексуальной активности) мужчин и женщин. Снижение гиперактивности у детей. Лечение витилиго в комплексе с фенилаланином. Восстановление нарушения функций щитовидной железы. Снижение аллергических реакций.
Также L-тирозин способствует выработке эндорфина и адреналина — гормонов, которые успокоительно влияют на нервную систему и помогают снизить тягу к кофеину, к спиртному, нейростимуляторам. Эта аминокислота обладает защитными функциями клеток нервной системы и головного мозга от последствий отравления алкоголем и табакокурения и применяется при лечении зависимости от алкоголя и лекарственных средств.
Так как с возрастом гормон мелатонин снижается, биологические добавки L-Tyrosine стимулируют его выработку. Это содействует укреплению иммунитета, нормализует циклы сна/бодрствования, выводит плохой холестерин у людей пожилого возраста.
При недостатке этой аминокислоты может даже понижаться температура тела. Вследствие этого возникает ощущение холода в руках и ногах, а также могут появиться судороги в икроножных мышцах. L-тирозин рекомендуется принимать людям, которые соблюдают диету с низким содержание белка в пище.
Л-тирозин отзывы
Прежде чем принять решение для приема любого препарата стоит познакомиться с рекомендациями тех, кто уже его принимал. Отзывы о тирозине в большинстве своем положительные и у этой биодобавки есть много поклонников.
Чаще всего препараты с этой аминокислотой принимают для улучшения своего эмоционального состояния. Например, один пользователь отмечает, что приём тирозина два раза в день помог ему справляться с апатией, усталостью и депрессией, у него улучшилось настроение и появились силы.
Чтобы побороть депрессию, подавленное настроение и лень, а также мотивировать себя на какую-то деятельность или спортивные тренировки аминокислоту Л-Тирозин принимают курсами.
Показать скрытое содержание
Отзывы спортсменов об этой аминокислоте показывают, что её действие схоже с Л-карнитином. Она важна для правильного распределения энергии при тренировках, помогает максимально сохранить набранную мышечную массу и легче переносить периоды сушки. Отзыв одного спортсмена: «С тирозином можно тренироваться хоть каждый день и хорошо себя чувствовать. Обычно принимаю до 120 капсул в течение 40 дней».
Также много отзывов об Л-Тирозине от людей, ведущих активный образ жизни. Недостаток этой аминокислоты приводит к ухудшению мозговой деятельности, замедлению обмена веществ и потере физических сил. Отзывы показывают, что в этом случае достаточно принимать курс БАД около двух месяцев по 2 таблетки в день и повторять его через месяца три. Принимать постоянно L-тирозин смысла нет.
Кроме того, некоторые отзывы хвалят л-тирозин по сравнению с другими ВСАА с богатым составом. Пользователи говорят, что есть ощутимая разница по эффекту — от него гораздо больше энергии и выносливости, быстрее восстанавливаются мышцы после нагрузок. Нормализуется аппетит, особенно после силовых тренировок.
Согласно отзывам, оптимальная норма для приёма — две капсулы в день по 500 мг чистого тирозина в составе. Одной банки хватает на два месяца, без каких-либо дополнительных добавок и витаминов.
Л тирозин отзывы для похудения. Нельзя не упомянуть отзывы о БАДе желающих похудеть. Например, по отзыву одной пользовательницы этот препарат заметно снизил аппетит уже через неделю приёма, кроме того, нет желания есть сладкое.
Нормализовался сон, стал крепким и спокойным, что тоже положительно сказывается на обмене веществ. Отзывы пожилых людей также показывают положительное действие аминокислоты на организм. Через год после употребления тирозина по три капсулы в день в перерывах между едой самочувствие становиться намного бодрее. И судя по одному отзыву даже поубавилась седина на отрастающих корнях волос.
Где л тирозин купить
 Приобрести натуральную биодобавку L-Tyrosine можно в интернете на специализированном сайте IHerb.
Приобрести натуральную биодобавку L-Tyrosine можно в интернете на специализированном сайте IHerb.
Один из самых популярных препаратов L-Tyrosine NOW (120 капсул с оптимальной дозировкой 500 мг). В состав биологической добавки американского производителя входят микроэлементы, которые повышают усвояемость аминокислоты и усиливают ее активность.
Препарат L-тирозин от Thorne Research помогает улучшить самочувствие, мыслительную деятельность и память, повысить стрессоустойчивость и снять усталость после больших физических и умственных нагрузок.
Действие вещества проявляется постепенно и после двух недель применения станут заметны положительные признаки улучшения. Благодаря аминокислоте Л тирозину возможно снижение приёма антидепрессантов.
Л тирозин цена Now Foods L-Tyrosine, 500 мг, 120 капсул можно посмотреть на сайте IHerb, где действует система скидок и акций.
Л-тирозин инструкция по применению
Л-тирозин как принимать. Стоит внимательно относиться к приёму препарата и не увеличивать указанных рекомендаций и дозировок. Вследствие неправильного употребления возникает риск проявления побочных действий.
L-тирозин принимается не более одной капсулы за 1 раз. В течение дня кратность приёма составляет от 1 до 3, в зависимости от цели и выраженности клинических проявлений. Запивать капсулу необходимо только чистой негазированной водой, достаточно 100-200 мл.
Л тирозин инструкция по применению для похудения предусматривает прием одной капсулы в день утром до еды. Этой дозировки достаточно для снижения аппетита, уменьшения жировой массы и улучшения обмена веществ.
Для лучшей всасываемости активного вещества и биодоступности аминокислоты следует принимать БАД за полчаса до еды. Рекомендуемый курс употребления аминокислоты Л-тирозина составляет месяц. При необходимости курс можно повторять через три или шесть месяцев.
Кроме того, существуют продукты богатые тирозином. Для пополнения запасов аминокислоты можно употреблять продукты, богатые белками: индейку; курицу; рыбу; фасоль; сою; молочные продукты; авокадо; миндаль и арахис; кунжутное семя.
При всех положительных свойствах препаратом с тирозином не стоит злоупотреблять.
Существуют некоторые противопоказания к применению биодобавки:
- беременность и кормление грудью;
- совмещение приема с другими антидепрессантами;
- шизофрения;
- гипертония;
- индивидуальная непереносимость компонентов;
- возраст до 18 лет.
Л-тирозин для щитовидной железы
Данная аминокислота способствует выработке в организме гормонов щитовидки тироксина и трийодтиронина. Именно недостаток этих гормонов может нарушить нормальное функционирование щитовидной железы.
Л-тирозин при гипотиреозе применяется для заместительной терапии. Суточная дозировка подбирается индивидуально в зависимости от тяжести гипотиреоза и от исследования уровня ТТГ. Людям с проблемами щитовидной железы не следует начинать употреблять Тирозин самостоятельно без консультации врача.
Через сколько часов выводится л-тирозин. Так как аминокислота имеет свойство медленно выводиться из организма, то её необходимое количество для поддержания уровня гормонов сохраняется надолго.
Итак, мы увидели, что Л-тирозин – это очень важная аминокислота, которая играет важную роль в функционировании эндокринной, сердечно-сосудистой систем. Она необходима для повышения стрессоустойчивости, борьбы с депрессиями, усталостью и рассеянностью.
ssvsport.ru
Тирозин (L-тирозин) | |
Как Вы думаете, существуют ли вещества, которые способны увеличить концентрацию Вашего внимания, повысить работоспособность, улучшить сон, облегчить влияние стресса, но при этом не имеющие никаких побочных действий, абсолютно природные и «родные» человеческому организму? Думаете, это травки из фитоаптеки? А вот и нет. Это аминокислоты – вещества, без которых не может выжить ни одно живое существо, т.к. именно они являются основным строительным материалом для любых белков в нашем организме. Также аминокислоты – основа для синтеза нейромедиаторов, обеспечивающих нам связь между нейронами головного мозга.
Я хочу подробнее остановиться на тирозине – аминокислоте, влияние которой на когнитивные функции человека, особенно во время стресса, научно доказано.
Тирозин был открыт в 1846 году немецким ученым Ю. Либихом, он выделил эту аминокислоту из белка сыра. Название свое тирозин получил именно от греческого «тирос» — сыр.
Структурная формула тирозина выглядит следующим образом:
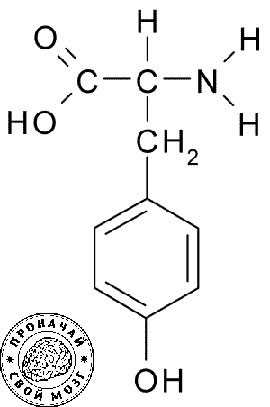 В организме человека присутствует в основном левосторонняя форма тирозина – левотирозин, или L-тирозин.
В организме человека присутствует в основном левосторонняя форма тирозина – левотирозин, или L-тирозин.
Из L-тирозина синтезируются дофамин и адреналин.
Основная функция дофамина — обеспечить человеку чувства удовольствия, удовлетворения, хорошее настроение. Он напрямую влияет на нашу мотивацию, уровень работоспособности, уменьшение боли, улучшение памяти. Недостаток L-тирозина, а, следовательно, и дофамина, приводит к депрессии, вялости, умственной заторможенности.
Также важное значение имеет количество норадреналина в организме. В условиях стресса он в огромных количествах преобразуется в адреналин, и когда возникает его нехватка, человек испытывает эмоциональное и интеллектуальное истощение, физическую слабость, у него скачет давление, возникает дрожь в конечностях. Прием тирозина в этом случае способен облегчить восприятие стресса и реакцию организма на него.
В каких продуктах содержится тирозин?
Прежде всего, это молочные продукты и яйца. Также значительное количество л-тирозина содержится в миндале, арахисе, кунжуте, тыквенных семечках. Из фруктов — бананы и авокадо.
К сожалению, современное высокоуглеводное питание не всегда способно удовлетворить суточную потребность в тирозине, которая составляет 16 мг на кг массы тела человека.
Купить тирозин вы можете в аптеке или в магазине спортивного питания. В основном это капсулы 500 мг. В день принимают по 1 капсуле, перед значительной физической или умственной нагрузкой, возможной стрессовой ситуацией можно принять от 500 до 2000 мг за 30-60 минут.
Внимание! Инструкция по применению тирозина содержит важное предостережение: запрещен одновременный прием л-тирозина и некоторых видов антидепрессантов.
Действие тирозина на организм:
- улучшает память, особенно в стрессовых ситуациях;
- облегчает восприятие стресса;
- сокращает количество гормонов стресса и улучшает самочувствие в период недосыпания, усталости, нервного перенапряжения;
- регулирует артериальное давление;
- облегчает самочувствие при отказе от курения, диетах;
- повышает работоспособность при синдроме хронической усталости;
- помогает преодолеть лень и хандру;
- уменьшает проявления вегетососудистой дистонии.
В общем, если Вам нужно «взбодрить» мозг и организм в целом – попробуйте тирозин.
Тирозин инструкция по применению
fitnessbrain.ru
Тирозин — Википедия (с комментариями)
Материал из Википедии — свободной энциклопедии
| Тирозин | |
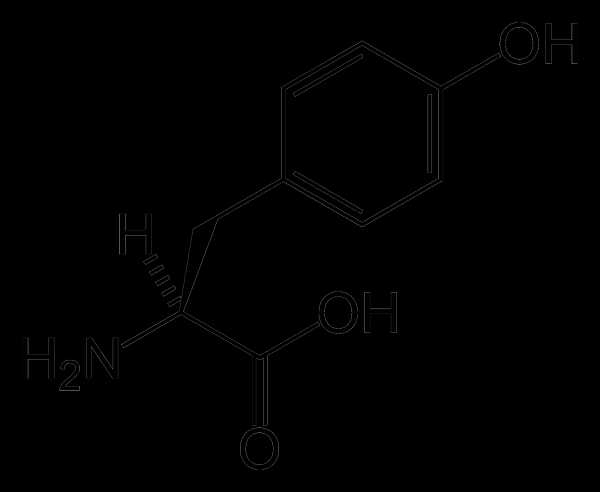 | |
| Общие | |
|---|---|
| Систематическое наименование | 2-амино-3-(4- |
| Сокращения | Тир, Tyr, Y UAU,UAC |
| Рац. формула | C9H11NO3 |
| Физические свойства | |
| Молярная масса | 181,19 г/моль |
| Плотность | 1,456 г/см³ |
| Термические свойства | |
| Т. плав. | 343 °C |
| Химические свойства | |
| pKa | 2,24 9,04 10,10 |
| Классификация | |
| Рег. номер CAS | [60-18-4] |
| Рег. номер EINECS | 200—460-4 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Тирози́н (α-амино-β-(п-гидроксифенил)пропионовая кислота, сокр.: Тир, Tyr, Y) — ароматическая альфа-аминокислота. Существует в двух оптически изомерных формах — L и D и в виде рацемата (DL). По строению соединение отличается от фенилаланина наличием фенольной гидроксильной группы в пара-положении бензольного кольца. Известны менее важные с биологической точки зрения мета— и орто— изомеры тирозина.
L-тирозин является протеиногенной аминокислотой и входит в состав белков всех известных живых организмов. Тирозин входит в состав ферментов, во многих из которых именно тирозину отведена ключевая роль в ферментативной активности и её регуляции. Местом атаки фосфорилирующих ферментов протеинкиназ часто является именно фенольный гидроксил остатков тирозина. Остаток тирозина в составе белков может подвергаться и другим посттрансляционным модификациям. В некоторых белках (резилин насекомых) присутствуют молекулярные сшивки, возникающие в результате посттрансляционной окислительной конденсации остатков тирозина с образованием дитирозина и тритирозина.
Окрашивание в результате ксантопротеиновой качественной реакции на белки определяется преимущественно нитрованием остатков тирозина (нитруются также остатки фенилаланина, триптофана, и гистидина).
Биосинтез
В процессе биосинтеза тирозина промежуточными соединениями являются шикимат, хоризмат, префенат. Из центральных метаболитов тирозин в природе синтезируют микроорганизмы, грибы и растения. Животные не синтезируют тирозин de novo, но способны гидроксилировать незаменимую аминокислоту фенилаланин в тирозин. Более подробно биосинтез тирозина рассмотрен в статье шикиматный путь.
Тирозин относят к заменимым для большинства животных и человека аминокислотам, так как в организме эта аминокислота образуется из другой (незаменимой) аминокислоты — фенилаланина.
Катаболизм
В организм животных и человека тирозин поступает с пищей. Также тирозин образуется из фенилаланина (реакция протекает в печени под действием фермента фенилаланин-4-гидроксилазы). Превращение фенилаланина в тирозин в организме в большей степени необходимо для удаления избытка фенилаланина, а не для восстановления запасов тирозина, так как тирозин обычно в достаточном количестве поступает с белками пищи, и его дефицита, как правило, не возникает. Избыток тирозина утилизируется. Тирозин путём переаминирования с α-кетоглутаровой кислотой превращается в 4-гидроксифенилпируват, который далее окисляется (с одновременной миграцией и декарбоксилированием кетокарбоксиэтильного заместителя) в гомогентизат. Гомогентизат через стадии образования 4-малеилацетоацетата и 4-фумарилацетоацетата распадается до фумарата и ацетоацетата. Окончательное разрушение происходит в цикле Кребса.
Таким образом, у животных и человека тирозин распадаются до фумарата (превращается в оксалоацетат, являющийся субстратом глюконеогенеза) и ацетоацетата (повышает уровень кетоновых тел в крови), поэтому тирозин, а также превращающийся в него фенилаланин, по характеру катаболизма у животных относят к глюко-кетогенным (смешанным) аминокислотам (см. классификацию аминокислот).
В природе известны и другие пути биодеградации тирозина.
Из тирозина синтезируются такие биологически активные вещества, как ДОФА, тиреоидные гормоны (тироксин, трийодтиронин). ДОФА является предшественником катехоламинов (дофамин, адреналин, норадреналин) и пигмента меланина. Гомогентизат является предшественником токоферолов, пластохинона (у организмов, способных синтезировать эти соединения).
С обменом тирозина связаны некоторые известные наследственные заболевания. При наследственном заболевании фенилкетонурии превращение фенилаланина в тирозин нарушено, и в организме происходит накопление фенилаланина и его метаболитов (фенилпируват, фениллактат, фенилацетат, орто-гидроксифенилацетат, фенилацетилглутамин), избыточное количество которых отрицательно сказывается на развитии нервной системы. При другом известном наследственном заболевании — алкаптонурии — нарушено превращение гомогентизата в 4-малеилацетоацетат.
Известно также несколько относительно редких заболеваний (тирозинемии), вызванных нарушениями обмена тирозина. Лечение этих заболеваний, как и фенилкетонурии — диетическое ограничение белка.
Применение
Тирозин подавляет аппетит, способствует уменьшению отложения жиров, способствует выработке меланина и улучшает функции надпочечников, щитовидной железы и гипофиза.К:Википедия:Статьи без источников (тип: не указан)[источник не указан 3203 дня]
См. также
Напишите отзыв о статье «Тирозин»
Литература
- Report of Medical Research Council on the Dietary Management of PKU. Recommendations on the Dietary Management of PKU. Arch. Dis. Child. 1993: 68; 426-7.
- Dixon M., MacDonald A, White F. Disorders of Amino Acid Metabolism, Organic Acidemias and Urea Cycle Defects PKU in Lawson M, Shaw V (eds.). Clinical Paediatric Dietetics. Oxford:Blackwell Science, 2001,p233-294.
- Holme E, Linstedt S. Tyrosinemia Type I adn NTBC (2-(2-nitro-4-triflourom othylbenoyl)-1,3-cyclohexanedione). J. Inherit. Metab. Dis. 1998:21;507-517.
- Ellaway CJ., Holme E, Standing S. et al. Outcome of Tyrosinemia Type III. J. Inherit. Metab. Dis 2001:24;824-32.
Отрывок, характеризующий Тирозин
– Не говорите мне про это. Что мне зa дело? – сказал он. – Я говорю, что безумно, безумно влюблен в вас. Разве я виноват, что вы восхитительны? Нам начинать.Наташа, оживленная и тревожная, широко раскрытыми, испуганными глазами смотрела вокруг себя и казалась веселее чем обыкновенно. Она почти ничего не помнила из того, что было в этот вечер. Танцовали экосез и грос фатер, отец приглашал ее уехать, она просила остаться. Где бы она ни была, с кем бы ни говорила, она чувствовала на себе его взгляд. Потом она помнила, что попросила у отца позволения выйти в уборную оправить платье, что Элен вышла за ней, говорила ей смеясь о любви ее брата и что в маленькой диванной ей опять встретился Анатоль, что Элен куда то исчезла, они остались вдвоем и Анатоль, взяв ее за руку, нежным голосом сказал:
– Я не могу к вам ездить, но неужели я никогда не увижу вас? Я безумно люблю вас. Неужели никогда?… – и он, заслоняя ей дорогу, приближал свое лицо к ее лицу.
Блестящие, большие, мужские глаза его так близки были от ее глаз, что она не видела ничего кроме этих глаз.
– Натали?! – прошептал вопросительно его голос, и кто то больно сжимал ее руки.
– Натали?!
«Я ничего не понимаю, мне нечего говорить», сказал ее взгляд.
Горячие губы прижались к ее губам и в ту же минуту она почувствовала себя опять свободною, и в комнате послышался шум шагов и платья Элен. Наташа оглянулась на Элен, потом, красная и дрожащая, взглянула на него испуганно вопросительно и пошла к двери.
– Un mot, un seul, au nom de Dieu, [Одно слово, только одно, ради Бога,] – говорил Анатоль.
Она остановилась. Ей так нужно было, чтобы он сказал это слово, которое бы объяснило ей то, что случилось и на которое она бы ему ответила.
– Nathalie, un mot, un seul, – всё повторял он, видимо не зная, что сказать и повторял его до тех пор, пока к ним подошла Элен.
Элен вместе с Наташей опять вышла в гостиную. Не оставшись ужинать, Ростовы уехали.
Вернувшись домой, Наташа не спала всю ночь: ее мучил неразрешимый вопрос, кого она любила, Анатоля или князя Андрея. Князя Андрея она любила – она помнила ясно, как сильно она любила его. Но Анатоля она любила тоже, это было несомненно. «Иначе, разве бы всё это могло быть?» думала она. «Ежели я могла после этого, прощаясь с ним, улыбкой ответить на его улыбку, ежели я могла допустить до этого, то значит, что я с первой минуты полюбила его. Значит, он добр, благороден и прекрасен, и нельзя было не полюбить его. Что же мне делать, когда я люблю его и люблю другого?» говорила она себе, не находя ответов на эти страшные вопросы.
Пришло утро с его заботами и суетой. Все встали, задвигались, заговорили, опять пришли модистки, опять вышла Марья Дмитриевна и позвали к чаю. Наташа широко раскрытыми глазами, как будто она хотела перехватить всякий устремленный на нее взгляд, беспокойно оглядывалась на всех и старалась казаться такою же, какою она была всегда.
После завтрака Марья Дмитриевна (это было лучшее время ее), сев на свое кресло, подозвала к себе Наташу и старого графа.
– Ну с, друзья мои, теперь я всё дело обдумала и вот вам мой совет, – начала она. – Вчера, как вы знаете, была я у князя Николая; ну с и поговорила с ним…. Он кричать вздумал. Да меня не перекричишь! Я всё ему выпела!
– Да что же он? – спросил граф.
– Он то что? сумасброд… слышать не хочет; ну, да что говорить, и так мы бедную девочку измучили, – сказала Марья Дмитриевна. – А совет мой вам, чтобы дела покончить и ехать домой, в Отрадное… и там ждать…
– Ах, нет! – вскрикнула Наташа.
– Нет, ехать, – сказала Марья Дмитриевна. – И там ждать. – Если жених теперь сюда приедет – без ссоры не обойдется, а он тут один на один с стариком всё переговорит и потом к вам приедет.
Илья Андреич одобрил это предложение, тотчас поняв всю разумность его. Ежели старик смягчится, то тем лучше будет приехать к нему в Москву или Лысые Горы, уже после; если нет, то венчаться против его воли можно будет только в Отрадном.
– И истинная правда, – сказал он. – Я и жалею, что к нему ездил и ее возил, – сказал старый граф.
– Нет, чего ж жалеть? Бывши здесь, нельзя было не сделать почтения. Ну, а не хочет, его дело, – сказала Марья Дмитриевна, что то отыскивая в ридикюле. – Да и приданое готово, чего вам еще ждать; а что не готово, я вам перешлю. Хоть и жалко мне вас, а лучше с Богом поезжайте. – Найдя в ридикюле то, что она искала, она передала Наташе. Это было письмо от княжны Марьи. – Тебе пишет. Как мучается, бедняжка! Она боится, чтобы ты не подумала, что она тебя не любит.
– Да она и не любит меня, – сказала Наташа.
– Вздор, не говори, – крикнула Марья Дмитриевна.
– Никому не поверю; я знаю, что не любит, – смело сказала Наташа, взяв письмо, и в лице ее выразилась сухая и злобная решительность, заставившая Марью Дмитриевну пристальнее посмотреть на нее и нахмуриться.
– Ты, матушка, так не отвечай, – сказала она. – Что я говорю, то правда. Напиши ответ.
Наташа не отвечала и пошла в свою комнату читать письмо княжны Марьи.
Княжна Марья писала, что она была в отчаянии от происшедшего между ними недоразумения. Какие бы ни были чувства ее отца, писала княжна Марья, она просила Наташу верить, что она не могла не любить ее как ту, которую выбрал ее брат, для счастия которого она всем готова была пожертвовать.
«Впрочем, писала она, не думайте, чтобы отец мой был дурно расположен к вам. Он больной и старый человек, которого надо извинять; но он добр, великодушен и будет любить ту, которая сделает счастье его сына». Княжна Марья просила далее, чтобы Наташа назначила время, когда она может опять увидеться с ней.
Прочтя письмо, Наташа села к письменному столу, чтобы написать ответ: «Chere princesse», [Дорогая княжна,] быстро, механически написала она и остановилась. «Что ж дальше могла написать она после всего того, что было вчера? Да, да, всё это было, и теперь уж всё другое», думала она, сидя над начатым письмом. «Надо отказать ему? Неужели надо? Это ужасно!»… И чтоб не думать этих страшных мыслей, она пошла к Соне и с ней вместе стала разбирать узоры.
wiki-org.ru
L-Тирозин [LifeBio.wiki]
Фармакологическая группа: [[аминокислоты|аминокислоты]]
Тирозин (сокращенно Tyr или Y), или 4-гидроксифенилаланин, является одной из 22 аминокислот, использующихся клетками для синтеза белков. Его кодоны – UAC и СХУ. Тирозин не является незаменимой аминокислотой и имеет полярную боковую цепь. Слово «тирозин» происходит от греческого «тири» (сыр), так как впервые эта аминокислота была обнаружена в 1846 году немецким химиком Юстусом фон Либихом в виде белка казеина, находящегося в сыре. Функциональная группа или боковая цепь аминокислоты называется тирозил.
L-Тирозин является [[аминокислоты|аминокислотой]], которая используется для производства норадреналина и дофамина; эта аминокислота действует в качестве антистрессового средства при остром стрессе (при котором снижается уровень адреналина) и может предотвращать вызванный стрессом дефицит памяти.
Функции
Кроме того, что тирозин является протеиногенной аминокислотой, он играет особую роль из-за функциональности фенола. Тирозин действует в качестве приемника фосфатных групп, которые передаются посредством протеинкиназ (так называемых рецепторных тирозинкиназ). Фосфорилирование гидроксильных групп изменяет активность белка-мишени. Остаток тирозина также играет важную роль в процессе фотосинтеза. В хлоропластах (фотосистеме II) он действует в качестве донора электронов в восстановлении окисленного хлорофилла. Здесь его фенольная OH-группа подвергается депротонированию. Затем радикал восстанавливают в фотосистему II четырьмя основными кластерами марганца.
Описание
L-тирозин является стимулирующей аминокислотой. Является одной из формЖиросжигателя
Ноотропного препарата
Добавки — заменителя аминокислот
L-тирозин инструкция по применению
Показания к применению: усталость и стресс (острый) Как правило, L-тирозин следует принимать в дозах 500-2000мг приблизительно за 30-60 минут до любого стресса (либо тренировки). Исследования позволяют предположить, что L-тирозин действует в качестве антистрессового средства в дозировке 100-150 мг/кг массы тела при приеме за 60 минут до тренировки. Интервал дозировки составляет 9-13.5г для человека весом около 200 фунтов, и 7-10 – для человека весом около150 фунтов. При использовании более высоких доз, с возникновением проблем с пищеварением, можно произвести разделение на две дозы, интервалом в полчаса (30 и 60 минут до стресса).
Источники и структура
Биологические свойства
Катехоламиновый метаболический путь in vivo начинается с аминокислоты L-фенилаланина, которая превращается в L-тирозин при участии фермента фенилаланин гидроксилазы. L-тирозин затем превращается в L-допу при помощи тирозин гидроксилазы. Леводопа затем подвергается декарбоксилированию при участии декарбоксилазы L-аминокислот, в дофамин, который затем превращается в норадреналин, посредством окисления ферментом дофамин-бета-гидроксилазы, а затем, наконец, превращается в адреналин с помощью фермента фенилэтаноламин-N-метил-трансферазы. Последние три соединения (дофамин, норадреналин и адреналин) в совокупности называются «катехоламинами».1) Применение любого из вышеперечисленных соединений позволяет увеличить уровень адреналина в организме. L-тирозин превращается в леводопу, которая затем превращается в активные катехоламины (адреналин, норадреналин и дофамин). Для устранения дефицита любого из перечисленных нейротрансмиттеров, L-тирозин используется в качестве субстрата.
Фенилкетонурия
Фенилкетонурия (ФКУ) является генетическим заболеванием, при котором организм не в состоянии должным образом усваивать аминокислоту фенилаланин, сопровождается накоплением фенилаланина до токсических уровней. Тирозин может смягчать симптомы фенилкетонурии (поскольку снижение уровня фенилаланина может вызывать уменьшение количества катехоламинов, однако этого можно избежать при приеме L-тирозина, в который превращается фенилаланин для создания катехоламинов). Но, пока что, эти результаты являются предварительными.2)
Пищевые источники
Тирозин, который также может быть синтезирован в организме из фенилаланина, содержится во многих богатых белками пищевых продуктах, таких как курица, индейка, рыба, арахис, миндаль, авокадо, молоко, сыр, йогурт, творог, фасоль, тыквенные семечки, кунжут, бананы и соевые продукты.
Биосинтез
Растения и большинство микроорганизмов производят тирозин с помощью префената, промежуточного вещества на шикиматном пути биозинтеза. Префенат окислительно декарбоксилируется с сохранением гидроксильной группы, для получения р-гидроксифенилпирувата, который трансаминируется с использованием глутамата в качестве источника азота, в результате чего получается тирозин и альфа-КГ. Млекопитающие синтезируют тирозин из незаменимой аминокислоты фенилаланина (Phe), добываемой из пищи. Превращение фенилаланина в тирозин катализируется ферментом гидроксилазы фенилаланина, монооксигеназной. Этот фермент катализирует реакцию, вызывая добавление гидроксильной группы в конец 6-углерод ароматического кольца фенилаланина, что, в конечном итоге, и создает тирозин.
Метаболизм
Фосфорилирование и сульфатирование
Некоторые из остатков тирозина могут быть объединены в фосфатную группу (то есть быть фосфорилированы) через протеинкиназу. Фосфорилированная форма тирозина называется фосфотирозином. Фосфорилирование тирозина считается одним из ключевых шагов в трансдукции сигнала и регулировании ферментативной активности. Фосфотирозин может быть обнаружен с помощью специфических антител. Остатки тирозина могут быть также модифицированы путем добавления сульфатной группы, этот процесс известен как сульфатирование тирозина. Сульфатирование тирозина катализируется тирозилпротеиновой сульфотрансферазой (TPST). Как и антитела фосфотирозина, о которых говорилось выше, недавно были описаны антитела, способные обнаруживать сульфотирозин.
Предшественник нейромедиаторов и гормонов
В дофаминергических клетках головного мозга тирозин превращается в леводопу под воздействием фермента гидроксилазы тирозина (TH). TH является ферментом, ограничивающим скорость, и участвующим в синтезе нейромедиатора дофамина. Дофамин затем может быть преобразован в катехоламин норадреналин и адреналин. Гормоны щитовидной железы трийодтиронин (Т3) и тироксин (Т4) в коллоидной системе щитовидной железы также производятся из тирозина.
Предшественник алкалоидов
Млечный сок растения Papaver Somniferum (опиумный мак) способен преобразовывать тирозин в морфин и этот био-путь осуществляется при участии углерод-14 радиоактивно меченого тирозина для того, чтобы проследить весь синтез в естественных условиях. Кактус, производящий мескалин, способен биосинтезировать тирозин в мескалин при его введении при помощи инъекций.
Предшественник природных фенолов
Тирозин аммиак-лиаза (TAL) является ферментом в метаболическом пути биосинтеза природных фенолов. Он превращает L-тирозин в p-кумаровую кислоту.
Предшественник пигментов
Тирозин также является предшественником пигмента меланина.
Распад
Распад L-тирозина (синоним пара-гидроксифениланина) начинается с трансаминирования, зависящего от а-кетоглютарата через тирозин трансаминазу в пара-гидроксифенилпируват. «Пара», сокращенно р, означает, что гидроксильные группы и боковые цепи на фенил кольце находятся напротив друг друга. В следующем шаге – окислении – происходит катализация р-гидроксифенилпируват -диоксигеназы и отщепление СО2 гомогентизата (2,5-дигидроксифенилуксусной кислоты). Для того, чтобы отделить гомогентизат от ароматического кольца, требуется дальнейшая диоксигеназа, гомогентизат-оксигеназа. Таким образом, путем включения молекулы O2, создается малеилацетоацетат. Фурамилацетат создается малеилацетоацетат-цис-транс-изомеразой при ротации карбоксильной группы, созданной из гидроксильной группы с помощью окисления. Эта цис-транс-изомераза использует глутатион в качестве кофермента. Фурамилацеоацетат, наконец, делится с помощью фурамилацетоацеат-гидролазы путем добавления молекулы воды. При этом высвобождаются фумарат (также являющийся метаболитом в цикле лимонной кислоты) и ацетоацетат (3-кетобутурат). Ацетоацетат является кетоновым телом, которое активируется сукцинил-КоА, а затем может быть преобразовано в ацетил-КоА, который, в свою очередь, может быть окислен циклом лимонной кислоты или использоваться для синтеза жирных кислот. Флоретиновая кислота является также мочевым метаболитом тирозина у крыс.
Бетаины
Орто-и мета-тирозин
Существует три изомера тирозина. В дополнение к общей аминокислоте L-тирозину, которая является пара-изомером (пара-тирозин, p-тирозин или 4-гидроксифенилаланин), существуют два дополнительных региоизомера, а именно – мета-тирозин (м-тирозин или 3- гидроксифенилаланин или L-m- тирозин) и орто-тирозин (о-тирозин или 2-гидроксифенилаланин), которые встречаются в природе. М-тирозин и о-тирозин, довольно редкие изомеры, возникают в результате неферментативного свободнорадикального гидроксилирования фенилаланина в условиях окислительного стресса. М-тирозин и его аналоги (редкие в природе, но доступные синтетически), применяют при лечении болезни Паркинсона, болезни Альцгеймера и артрита.
Медицинское использование тирозина
Тирозин является предшественником некоторых нейромедиаторов. Он увеличивает уровни нейромедиаторов в плазме (в частности, дофамина и норадреналина), но не оказывает практически никакого влияния на настроение. Влияние на настроение более заметно у людей, подвергающихся стрессу. В ряде исследований было показано, что тирозин может быть использован в таких ситуациях, как стресс, холод, усталость, потеря любимого человека (смерть или развод), длительная работа и лишение сна, так как он вызывает уменьшение уровней гормонов стресса, снижает вызванную стрессом потерю веса, что было доказано в испытаниях на животных; а также улучшает когнитивную и физическую работоспособность, что было показано в испытаниях на людях. Однако в связи с тем, что тирозингидроксилаза является ферментом, ограничивающим скорость, тирозин проявляет меньшие эффекты, чем L-допа. В нормальных условиях Тирозин не оказывает существенного влияния на настроение, когнитивные функции или физическую работоспособность человека. Суточная доза для клинического анализа, указанная в литературе, составляет около 100 мг / кг для взрослого, то есть около 6,8 грамм на 150 фунтов. Обычная дозировка до 500-1500 мг в день (доза, предложенная большинством производителей, обычно эквивалентна 1-3 капсулам чистого тирозина). Не рекомендуется превышать дозу в 12000 мг (12 г) в день. В самом деле, чрезмерные дозировки вызывают снижение уровня допамина в организме. Тирозин может уменьшить поглощение других аминокислот при высоких или хронических дозах. Это снижает поглощение L-допа.
Фармакология
Сыворотка
150 мг/кг L-тирозина, смешанного с яблочным пюре, может повысить концентрацию L-тирозина в плазме с 56.3 нмоль/л (базовые показатели) до 140-168 нмоль/л в течение 90 минут. Показатели оставались в пределах этой концентрации до прекращения измерений на 150 минуте. Существенное отличие от плацебо длилось в течение 30 минут и составило примерно 80нмоль/л. Данные изменения концентрации тирозина в плазме не сравнивали с увеличением уровня норадреналина в плазме, которое оказалось схожим в разных группах.3) Аналогичный всплеск содержания тирозина в сыворотке крови был отмечен у крыс (сыворотка не тестировалась на содержание норадреналина), и увеличение содержания тирозина в сыворотке длилось 4 часа, а затем показатели вернулись к своему исходному уровню.4) Тирозин довольно быстро всасывается из кишечника в кровь, и удерживается на высоком уровне в течение 2-4 часов после приема.
Воздействие на организм
Неврология
Механизмы
Поскольку L-тирозин предстает в роли предшественника нейромедиаторов норадреналина и дофамина, он непосредственно ускоряет процесс синтеза катехоламинов.5)
Память
L-тирозин (200-400мг/кг) может значительно повысить концентрацию норадреналина (также известного как норэпинефрин или НЭ) в гипофизе и предотвратить острое снижение концентрации НЭ у крыс, подверженных воздействию холода. Это может быть связано с тем, что L-тирозин может обращать потерю памяти у человека, вызванную стрессом во время нахождения организма в холодных условиях. Это исследование (n = 8) показало, что 150 мг / кг L-тирозина (растворенного в яблочном пюре, употребленного внутрь, при этом плацебо-группе давали просто яблочное пюре без добавок) проводилось в помещении, где температура была снижена с 22 ° С до +4 ° С. Тестируемые, которым давали L-тирозин, справились с заданием за более короткий отрезок времени и увеличили количество правильных ответов в условиях холода. Однако, при смене температур на более высокие, разница между группами была не такой выразительной (L-тирозин не способствовал дальнейшему улучшению производительности).6) В настоящее время нет доказательств того, что добавка L-тирозин может улучшить функцию памяти по сравнению с исходной, но в стрессовом состоянии может ослабить ухудшение памяти.
Внимание
Исследование с участием детей с диагнозом СДВГ показало, что сочетание добавки тирозина и 5-HTP (дозы были титрованными, при этом самое низкое содержание – 1,500мг тирозина и 150 мг 5-HTP, а самое высокое – 3,750мг и 425мг соответственно), выявило, что использование добавок привело к значительному сокращению симптомов по оценке СДВГ-RS; в этом исследование также использовался ряд других питательных веществ (1000 мг витамина С, 220 мг цитрата кальция, 75 мг витамина В6, 400 мкг фолиевой кислоты, 500 мг L-Лизина, 2,500-4,500мг L-цистеина и 200-400мг селена).7) Хотя L-тирозин значительно улучшает внимательность, на данный момент это не было достаточно протестировано. Были рассмотрены лишь единичные случаи, таким образом, невозможно с точностью определить, каким является его влияние.
Бодрость
Исследование L-тирозина, в котором применялось «продолжительное бодрствование», показало, что 150 мг / кг L-тирозина ослабляет снижение когнитивных функций, связанное с недостатком сна.8) L-тирозин может улучшить когнитивные функции во время бессонницы, не оказывая существенного влияния на сон.
Стресс
Острое неконтролируемое напряжение, которое способно истощить содержание концентрации норэпинефрина (НЭ) в нервной ткани, особенно в гипоталамусе и стволе мозга (содержащем голубые пятна), и поведенческие изменения, связанные с истощением НЭ были зафиксированы в исследовании поведения животных, проявившихся в качестве побега, спонтанной двигательной активности, агрессивного поведения, и плавания. Кратковременный неконтролируемый стресс – это феномен, благодаря которому может снижаться уровень норепинефрина в нервной ткани, особенно в гипоталамусе и мозговом стволе. У животных недостаток норепинефрина приводит к развитию спонтанной моторной активности, поведению, связанному с уклонением и избеганием, агрессивному поведению. Прием L-тирозина может смягчить развитие поведенческих отклонений, связанных с острыми неконтролируемыми факторами стресса у лабораторных животных, в диапазоне доз 200 -400мг / кг (перорально или внутривенно) за 30-60 минут до стрессовой ситуации.9) L-тирозин смягчает некоторые явные признаки острого и неконтролируемого стресса (в отличие от адаптогенных молекул, которые могут быть эффективны против хронического и контролируемого стресса). Некоторые исследования были проведены специально в условиях холодового стресса (так называемая «холодная терапия»). Было отмечено уменьшение времени неподвижности в зависимости от дозировки, у мышей с использованием инъекции 200-400 мг/ кг L-тирозина или 5- 20мг / кг фенилпропаноламина. Тирозин синергически сократил время неподвижности, при совместном приеме либо с фенилпропаноламином, либо с амфетамином. Эти эффекты кореллируют с концентрацией норадреналина в гипофизе, которая сохраняется на должном уровне с использованием L-тирозина. Эти защитные эффекты были отмечены в исследовании человека. Данная добавка также уменьшает негативные последствия холодового стресса, и существуют доказательства, выявленные при обследовании людей (влияние на функции памяти). 10) Одно исследование, проведенное на людях, показало высокий уровень защитного действия L-тирозина против острого стресса. Наблюдалось уменьшение симптомов острого перенапряжения, при этом прием 100 мг / кг L-тирозина (в два приема, интервалом в час) был связан с уменьшением головной боли, стресса, усталости, апатии, сонливости, мышечной боли. Это исследование также отметило улучшения (по отношению к плацебо) в общих показателях настроения и счастья и когнитивных функций. Подобные исследования с использованием той же пероральной дозы после сильного шумового напряжения, отметили быстрое снижение острого стресса.11) В исследовании с проведением недельной силовой тренировки было отмечено положительное воздействие, снятие напряжения у испытуемых с использованием 42г белка (2 г из которых составлял тирозин), наблюдалось сохранение когнитивных функций, однако не удалось обнаружить существенных улучшений в настроении у испытуемых.
Старение нейронов
Повышение уровня L-тирозина в мозге в настоящее время рассматривается в качестве фармацевтического способа облегчения неврологических ухудшений, поскольку снижение катехоламинов связано с деменцией.12) Удивительно, но катехоламины являются нейропротекторами и могут выступать в качестве антиоксидантов в головном мозге.
Сердечнососудистые заболевания
Артериальное давление
При приеме 150 мг / кг L-тирозина до когнитивного теста (в состоянии острого напряжения) не наблюдается значительного влияния на кровяное давление или на всплеск кровяного давления, вызванный острым стрессом. Тестирование курсантов, проходящих боевую подготовку, и потреблявших 42 г белка (2 г тирозин были смешаны с другими аминокислотами), выявило, что данная добавка снизила систолическое артериальное давление на 10,4% по сравнению с исходным уровнем. В группе плацебо наблюдалось меньшее и незначительное снижение кровяного давления. Никаких существенных изменений не отмечено и в диастолическом давлении, однако была отмечена тенденция к снижению. В другом исследовании при остром шумовом напряжении, выяснилось, что прием L-тирозина снижет диастолическое артериальное давление в течение 15 минут после приема препарата внутрь в дозе 100 мг /кг. Это снижение диастолического артериального давления было отмечено ранее в опытах над животными. 13) Хотя существует не достаточно надежных данных о препарате, похоже, что L-тирозин неэффективно понижает артериальное давление. Исследования были проведены в условиях стресса (повышенное артериальное давление), поэтому эффекты L-тирозина нельзя рассматривать отдельно от особенностей реакций организма на стресс.
L-тирозин и производительность
L-тирозин, как правило, используется совместно с чем-либо для облегчения снижения неврологической производительности, связанной с умеренным, либо долгосрочным умственным напряжением (при умственных или физических нагрузках). Существует предположение, что при увеличении нагрузки на нервную систему наблюдается увеличение производительности, хотя такое явление нельзя назвать систематическим. 14)
Формы L-тирозина
N-ацетил-L-тирозин (NALT)
N-ацетил-L-тирозин может жертвовать свободный L-тирозин in vivo после внутривенного применения, однако вызывает лишь 20% увеличение L-тирозина, несмотря на гораздо более выраженное увеличение сывороточных уровней NALT. 56% дозы NALT выводится из организма в моче в виде NALT, а не L-тирозина.15)
Доступность:
Список использованной литературы:
1) Nakashima A, et al. Role of N-terminus of tyrosine hydroxylase in the biosynthesis of catecholamines. J Neural Transm. (2009) 2) Poustie VJ, Rutherford P. Tyrosine supplementation for phenylketonuria. Cochrane Database Syst Rev. (2000) 3) Shurtleff D, et al. Tyrosine reverses a cold-induced working memory deficit in humans. Pharmacol Biochem Behav. (1994) 4) Topall G, Laborit H. Brain tyrosine increases after treating with prodrugs: comparison with tyrosine. J Pharm Pharmacol. (1989) 5) Lehnert H, Wurtman RJ. Amino acid control of neurotransmitter synthesis and release: physiological and clinical implications. Psychother Psychosom. (1993) 6) Shurtleff D, et al. Tyrosine reverses a cold-induced working memory deficit in humans. Pharmacol Biochem Behav. (1994) 7) Treatment of attention deficit hyperactivity disorder with monoamine amino acid precursors and organic cation transporter assay interpretation 8) Neri DF, et al. The effects of tyrosine on cognitive performance during extended wakefulness. Aviat Space Environ Med. (1995) 9) Banderet LE, Lieberman HR. Treatment with tyrosine, a neurotransmitter precursor, reduces environmental stress in humans. Brain Res Bull. (1989) 10) Dollins AB, et al. L-tyrosine ameliorates some effects of lower body negative pressure stress. Physiol Behav. (1995) 11) Deijen JB, et al. Tyrosine improves cognitive performance and reduces blood pressure in cadets after one week of a combat training course. Brain Res Bull. (1999) 12) Jodko K, Litwinienko G. Oxidative stress in the neurodegenerative diseases–potential antioxidant activity of catecholamines. Postepy Biochem. (2010) 13) Tyrosine administration reduces blood pressure and enhances brain norepinephrine release in spontaneously hypertensive rats 14) Meeusen R, Watson P, Dvorak J. The brain and fatigue: new opportunities for nutritional interventions. J Sports Sci. (2006) 15) Hoffer LJ, et al. N-acetyl-L-tyrosine as a tyrosine source in adult parenteral nutrition. JPEN J Parenter Enteral Nutr. (2003)
тирозин.txt · Последние изменения: 2016/04/06 15:51 — nataly
lifebio.wiki
Тирозин — это… Что такое Тирозин?
Тирози́н (α-амино-β-(п-гидроксифенил)пропионовая кислота, сокр.: Тир, Tyr, Y) — ароматическая альфа-аминокислота. Существует в двух оптически изомерных формах — L и D и в виде рацемата (DL). По строению соединение отличается от фенилаланина наличием фенольной гидроксильной группы в пара-положении бензольного кольца. Известны менее важные с биологической точки зрения мета— и орто— изомеры тирозина.
L-тирозин является протеиногенной аминокислотой и входит в состав белков всех известных живых организмов. Тирозин входит в состав ферментов, во многих из которых именно тирозину отведена ключевая роль в ферментативной активности и её регуляции. Местом атаки фосфорилирующих ферментов протеинкиназ часто является именно фенольный гидроксил остатков тирозина. Остаток тирозина в составе белков может подвергаться и другим посттрансляционным модификациям. В некоторых белках (резилин насекомых) присутствуют молекулярные сшивки, возникающие в результате посттрансляционной окислительной конденсации остатков тирозина с образованием дитирозина и тритирозина.
Окрашивание в результате ксантопротеиновой качественной реакции на белки определяется преимущественно нитрованием остатков тирозина (нитруются также остатки фенилаланина, триптофана, и гистидина).
Биосинтез
В процессе биосинтеза тирозина промежуточными соединениями являются шикимат, хоризмат, префенат. Из центральных метаболитов тирозин в природе синтезируют микроорганизмы, грибы и растения. Животные не синтезируют тирозин de novo, но способны гидроксилировать незаменимую аминокислоту фенилаланин в тирозин. Более подробно биосинтез тирозина рассмотрен в статье шикиматный путь.
Тирозин относят к заменимым для большинства животных и человека аминокислотам, так как в организме эта аминокислота образуется из другой (незаменимой) аминокислоты — фенилаланина.
Катаболизм
В организм животных и человека тирозин поступает с пищей. Также тирозин образуется из фенилаланина (реакция протекает в печени под действием фермента фенилаланин-4-гидроксилазы). Превращение фенилаланина в тирозин в организме в большей степени необходимо для удаления избытка фенилаланина, а не для восстановления запасов тирозина, так как тирозин обычно в достаточном количестве поступает с белками пищи, и его дефицита, как правило, не возникает. Избыток тирозина утилизируется. Тирозин путём переаминирования с α-кетоглутаровой кислотой превращается в 4-гидроксифенилпируват, который далее окисляется (с одновременной миграцией и декарбоксилированием кетокарбоксиэтильного заместителя) в гомогентизат. Гомогентизат через стадии образования 4-малеилацетоацетата и 4-фумарилацетоацетата распадается до фумарата и ацетоацетата. Окончательное разрушение происходит в цикле Кребса. Таким образом, у животных и человека тирозин распадаются до фумарата (превращается в оксалоацетат, являющийся субстратом глюконеогенеза) и ацетоацетата (повышает уровень кетоновых тел в крови), поэтому тирозин, а также превращающийся в него фенилаланин, по характеру катаболизма у животных относят к глюко-кетогенным (смешанным) аминокислотам (см. классификацию аминокислот).
В природе известны и другие пути биодеградации тирозина.
Из тирозина синтезируются такие биологически активные вещества, как ДОФА, тиреоидных гормонов (тироксин, трийодтиронин). ДОФА являетя предшественником катехоламинов (дофамин, адреналин, норадреналин) и пигмента меланина. Гомогентизат является предшественником токоферолов, пластохинона (у организмов, способных синтезировать эти соединения).
С обменом тирозина связаны некоторые известные наследственные заболевания. При наследственном заболевании фенилкетонурии превращение фенилаланина в тирозин нарушено, и в организме происходит накопление фенилаланина и его метаболитов (фенилпируват, фениллактат, фенилацетат, орто-гидроксифенилацетат, фенилацетилглутамин), избыточное количество которых отрицательно сказывается на развитии нервной системы. При другом известном наследственном заболевании — алкаптонурии — нарушено превращение гомогентизата в 4-малеилацетоацетат.
Известно также несколько относительно редких заболеваний (тирозинемии), вызванных нарушениями обмена тирозина. Лечение этих заболеваний, как и фенилкетонурии — диетическое ограничение белка.
Применение
Тирозин подавляет аппетит, способствует уменьшению отложения жиров, способствует выработке меланина и улучшает функции надпочечников, щитовидной железы и гипофиза.[источник не указан 818 дней]
См. также
Литература
- Report of Medical Research Council on the Dietary Management of PKU. Recommendations on the Dietary Management of PKU. Arch. Dis. Child. 1993: 68; 426-7.
- Dixon M., MacDonald A, White F. Disorders of Amino Acid Metabolism, Organic Acidemias and Urea Cycle Defects PKU in Lawson M, Shaw V (eds.). Clinical Paediatric Dietetics. Oxford:Blackwell Science, 2001,p233-294.
- Holme E, Linstedt S. Tyrosinemia Type I adn NTBC (2-(2-nitro-4-triflourom othylbenoyl)-1,3-cyclohexanedione). J. Inherit. Metab. Dis. 1998:21;507-517.
- Ellaway CJ., Holme E, Standing S. et al. Outcome of Tyrosinemia Type III. J. Inherit. Metab. Dis 2001:24;824-32.
dic.academic.ru

 Описание товара. Рекомендации по применению. Отзывы. Подробнее >>
Описание товара. Рекомендации по применению. Отзывы. Подробнее >>